题目内容
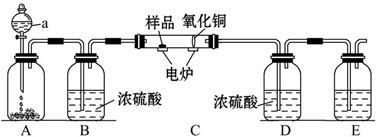
如图装置是用燃烧法来确定有机物组成的常用装置,这种方法是在电炉加热时用纯氧氧化管内样品,根据产物的质量确定有机物的组成(已知:C中的氧化铜是确保有机物中的碳元素完全转化为二氧化碳;A中的反应为2H2O2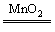 2H2O
2H2O
+O2↑)。
回答下列问题:
(1)a中盛放的物质是________;
(2)若去掉B装置会对什么元素的测量结果有影响?________,会使测量结果________(填“偏大”或“偏小”);
(3)E装置中所盛放物质最好选用__________(选填①氢氧化钙溶液 ②氢氧化钠溶液 ③水);
(4)若准确称取1.12 g样品(样品只含C、H、O三种元素中的两种或三种)。经充分燃烧后,D装置增重1.44 g,E装置增重3.52 g,则该有机物样品中所含的元素为________。
【解析】本题是用燃烧的方法来探究有机物中碳、氢、氧等元素的存在。将碳元素转化为二氧化碳,氢元素转化为水,通过检验生成物中二氧化碳和水的存在,来确定碳、氢元素的存在,由图示可知,B的作用是除去氧气中的水蒸气,D的作用是吸收反应生成的水, E的作用是吸收反应生成的二氧化碳;(1)A装置是用过氧化氢溶液和二氧化锰反应制氧气的装置,因而a中盛放的是过氧化氢溶液;(2)若去掉B装置,从A中挥发出来的水会进入D中,造成氢元素的测量结果偏大;(3)E装置中所盛放物质最好选用氢氧化钠溶液,因为氢氧化钠溶液可以完全吸收反应生成的二氧化碳;(4)D装置增重1.44 g,说明反应生成了1.44 g水;E装置增重3.52 g,说明反应生成了3.52 g二氧化碳。1.44 g水中氢元素的质量为 , 3.52 g二氧化碳中碳元素的质量为
, 3.52 g二氧化碳中碳元素的质量为 ,有机物样品中碳元素和氢元素的质量和为0
,有机物样品中碳元素和氢元素的质量和为0 .16 g+
.16 g+
0.96 g=1.12 g,说明该样品中只含有碳元素和氢元素。
答案:(1)过氧化氢溶液(或双氧水)
(2)氢元素 偏大 (3)② (4)碳元素、氢元素

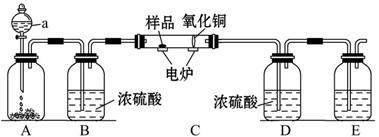
 图为实验室常用的制取氧气的实验装置,仔细观察后回答下列问题:
图为实验室常用的制取氧气的实验装置,仔细观察后回答下列问题: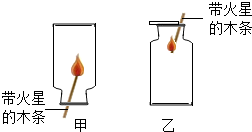
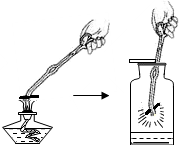
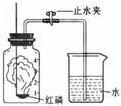 某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究.
某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究.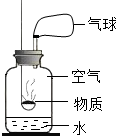 某校化学兴趣小组同学做镁带在空气中燃烧的实验时,发现白色生成物中混有少量淡黄色固体.针对这一现象,他们开展了如下实验探究.请仔细阅读并完成下列探究报告.
某校化学兴趣小组同学做镁带在空气中燃烧的实验时,发现白色生成物中混有少量淡黄色固体.针对这一现象,他们开展了如下实验探究.请仔细阅读并完成下列探究报告.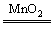 2H2O
2H2O