题目内容
某同学设计了四种物质的实验方案,其中理论上正确,操作上可行的是( )
A.CuO
| ||||||
B.Fe
| ||||||
C.Zn
| ||||||
D.CaCO3(块状)
|
A、氧化铜会与稀盐酸反应,生成氯化铜(盐)和水,酸和金属氧化物反应生成盐和水.铁可以置换出氯化铜溶液中的铜.反应式分别如下:CuO+HCl=CuCl2+H2O、CuCl2+Fe=Cu+FeCl2;故A选项可以;
B、铁在氧气中燃烧生成四氧化三铁,而不是氧化亚铁.故B选项不可以;
C、实验室常用锌与稀硫酸反应制取氢气,反应式为:Zn+H2SO4=ZnSO4+H2↑;氢气具有还原性,Cu2(OH)2CO3受热分解后产物CuO再与氢气反应:Cu2(OH)2CO3
2CuO+H2O+CO2↑、CuO+H2
Cu+H2O,故C选项可以;
D、碳酸钙与稀硫酸反应后生成硫酸钙,微溶于水,比较容易损害仪器;另外反应后硫酸钙在块状碳酸钙外形成保护层阻碍其继续与硫酸反应,反应不完全.故D选项不行.
故选AC
B、铁在氧气中燃烧生成四氧化三铁,而不是氧化亚铁.故B选项不可以;
C、实验室常用锌与稀硫酸反应制取氢气,反应式为:Zn+H2SO4=ZnSO4+H2↑;氢气具有还原性,Cu2(OH)2CO3受热分解后产物CuO再与氢气反应:Cu2(OH)2CO3
| ||
| ||
D、碳酸钙与稀硫酸反应后生成硫酸钙,微溶于水,比较容易损害仪器;另外反应后硫酸钙在块状碳酸钙外形成保护层阻碍其继续与硫酸反应,反应不完全.故D选项不行.
故选AC

练习册系列答案
相关题目
某同学设计了四种物质的实验方案,其中理论上正确,操作上可行的是( )
A、CuO
| ||||||
B、Fe
| ||||||
C、Zn
| ||||||
D、CaCO3(块状)
|
某同学设计了四种物质制备的实验方案,其中理论上正确,操作上可行的是( )
A、Fe
| ||||
B、CuO
| ||||
C、H2O
| ||||
D、CaCO3
|
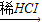 →CuCl2
→CuCl2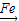 Cu
Cu Fe2O3
Fe2O3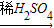 Fe2(SO4)3溶液
Fe2(SO4)3溶液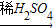 H2
H2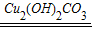 Cu
Cu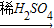 CO2
CO2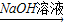 Na2CO3溶液
Na2CO3溶液