题目内容
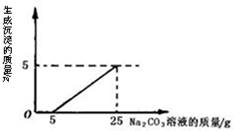 实验室废液桶中收集到大量含有的盐酸与氯化钙的废液(不考虑其他杂质).同学们测定该废液中含氯化钙的质量分数,他们取100g废液向其中慢慢滴加质量分数为26.5%的Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如图所示.
实验室废液桶中收集到大量含有的盐酸与氯化钙的废液(不考虑其他杂质).同学们测定该废液中含氯化钙的质量分数,他们取100g废液向其中慢慢滴加质量分数为26.5%的Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如图所示.(1)在加入Na2CO3溶液的过程中,开始时没有发现沉淀生成的原因是
(2)求废液中含氯化钙的浓度.
分析:(1)根据滴入的碳酸钠先与盐酸发生了反应氯化钠、水和二氧化碳进行解答;
(2)根据生成沉淀的质量就是碳酸钙的质量.利用碳酸钙的质量求出氯化钙的质量,进而求出废液中含氯化钙的浓度即可.
(2)根据生成沉淀的质量就是碳酸钙的质量.利用碳酸钙的质量求出氯化钙的质量,进而求出废液中含氯化钙的浓度即可.
解答:解:(1)开始时没有发现沉淀生成,说明Na2CO3溶液没有和CaCl2溶液反应,而是滴入的碳酸钠与盐酸发生了反应;故填:滴入的碳酸钠与盐酸发生了反应;
(2)设废液中氯化钙的质量为x,
Na2CO3+CaCl2═CaCO3↓+2NaCl
111 100
x 5g
=
x=5.55g
废液中含氯化钙的浓度=
×100%=5.55%
废液中含氯化钙的浓度为5.55%.
(2)设废液中氯化钙的质量为x,
Na2CO3+CaCl2═CaCO3↓+2NaCl
111 100
x 5g
| 111 |
| x |
| 100 |
| 5g |
x=5.55g
废液中含氯化钙的浓度=
| 5.55g |
| 100g |
废液中含氯化钙的浓度为5.55%.
点评:本题主要考查学生运用化学方程式和溶质质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目