��Ŀ����
����Ŀ����һ�ձ���ʢ��21.2gCaCO3��CaCl2�ķ�ĩ״���������м���178.8gˮ��ʹ������еĿ�������ȫ�ܽ⣬Ȼ������������μ������ʵ���������Ϊ20%��ϡ���ᣬ�ձ��зų������������������ϡ�����������ϵ������ͼ��ʾ��
���������ش��������⣺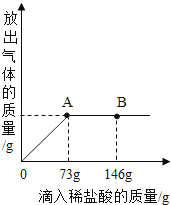
��1���ڵ���ϡ����Ĺ����У��۲쵽��һ������ʵ����������
��2�����μ���20%��ϡ������ͼ��A��ʱ���ձ�����Һ�ﺬ�е���������д��ѧʽ����
��3��������20%��ϡ����73gʱ����B�㣩����ͨ�����㣬���ʱ�ձ������ò�������Һ�����ʵ���������������ȷ��0.1g����
���𰸡�
��1����ɫ�����ܽ⣬��������
��2��CaCl2
��3��23.4g
���������⣺��1���ڵ���ϡ����Ĺ����У��۲쵽��һ������ʵ�������ǰ�ɫ�����ܽ⣬�������ݣ������ɫ�����ܽ⣬�������ݣ�
��2�����μ���20%��ϡ������ͼ��A��ʱ��̼��ƺ�ϡ����ǡ����ȫ��Ӧ���ձ�����Һ�ﺬ�е�������CaCl2 �� ���CaCl2 ��
��3����̼�������Ϊx�������Ȼ�������Ϊy��
CaCO3+2HCl �T CaCl2+H2O+CO2����
100 73 111
x 73g��20% y![]()
x=20g��y=22.2g��
��ʱ�ձ������ò�������Һ�����ʵ�����Ϊ��21.2g��20g+22.2g=23.4g��
�𣺵�����20%��ϡ����73gʱ���ձ������ò�������Һ�����ʵ�������23.4g��
���23.4g��
̼��ƺ�ϡ���ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼������ͼ����Ϣ����Ӧ�Ļ�ѧ����ʽ���ṩ�����ݿ��Խ�����ط���ļ�����жϣ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�