题目内容
根据质量守恒定律,化学反应前后不发生改变的是
- A.分子个数
- B.物质种类
- C.分子种类
- D.元素种类
D
分析:在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.这就叫做质量守恒定律.化学反应的过程,就是参加反应的各物质(反应物)的原子,重新组合而生成其他物质的过程.在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变.
解答:A、根据质量守恒定律,在化学反应前后,分子的个数可能改变,故A错误;
B、判断一个反应是否为化学反应的依据是反应是否生成新的物质,因此化学反应前后物质的种类一定改变,故B错误;
C、在化学反应中,分子破裂成原子,原子重新排列组合生成新物质.判断一个反应是否为化学反应的依据是反应是否生成新的物质.生成了新的物质,那么分子的种类必然改变,故C错误;
D、根据质量守恒定律可知,在化学反应中,反应前后元素种类没有改变,故D正确.
故选D.
点评:熟练掌握化学反应中的变与不变,会运用化学中的基本原理质量守恒定律处理问题,从而培养学生的创新思维能力.
分析:在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.这就叫做质量守恒定律.化学反应的过程,就是参加反应的各物质(反应物)的原子,重新组合而生成其他物质的过程.在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变.
解答:A、根据质量守恒定律,在化学反应前后,分子的个数可能改变,故A错误;
B、判断一个反应是否为化学反应的依据是反应是否生成新的物质,因此化学反应前后物质的种类一定改变,故B错误;
C、在化学反应中,分子破裂成原子,原子重新排列组合生成新物质.判断一个反应是否为化学反应的依据是反应是否生成新的物质.生成了新的物质,那么分子的种类必然改变,故C错误;
D、根据质量守恒定律可知,在化学反应中,反应前后元素种类没有改变,故D正确.
故选D.
点评:熟练掌握化学反应中的变与不变,会运用化学中的基本原理质量守恒定律处理问题,从而培养学生的创新思维能力.

练习册系列答案
相关题目
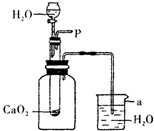 37、某校化学兴趣小组在了解农业生产中的化学时,了解到养鱼的农民有时会向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙
37、某校化学兴趣小组在了解农业生产中的化学时,了解到养鱼的农民有时会向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙