��Ŀ����
����Ŀ�������������������������������й㷺��Ӧ�ã���ʶ�������������������Ǹ��õ����ý�����
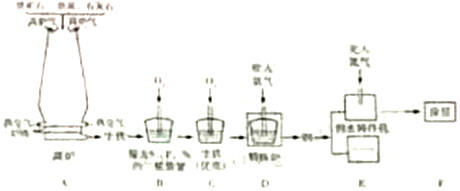
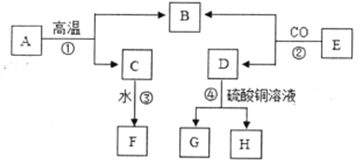
��1�������ڳ��л�ѧʵ���ж�γ��֣���ͼչʾ�˹���������һϵ�б仯��
![]()
�������仯���з�����Ӧ�Ļ�ѧ����ʽ��____��
�������仯���г�ȥ����Ļ�ѧ����ʽΪ____��
�����������a��b��c�ֱ������������������ʴ���������������������ǵ������ɴ�С��˳��Ϊ____������ĸ��ʾ����
��2�����м���ʵ�鷽���У���������֤����ͭ�������ֽ����Ļ��˳�����____������ţ�
�ٽ��������ֱ���뵽����ͭ��Һ�� �ڽ����ֱ���뵽������������ͭ��Һ��
�۽�ͭ�����ֱ���뵽��������Һ�� �ܽ�ͭ�ֱ���뵽����������������Һ��
�ݽ�����������ͭ��Һ����ͭ������������Һ��
��3�����Ȼ�ͭ���Ȼ������Ļ����Һ�м���һ������þ�ۣ���ַ�Ӧ����ˣ��õ���������Һ��ͨ���������жϣ�
����Һ��һ�����е�������____���ѧʽ����
���������еμ�ϡ���ᣬ�����ݲ�������������һ�����е�������____���ѧʽ����
���𰸡� Fe+CuSO4=FeSO4+Cu�� Fe2O3+6HCl=2FeCl3+3H2O�� b��a��c�� �٢ܢݣ� MgCl2�� Cu��Fe��
����������1���������仯��������������ͭ��Ӧ����ͭ������������������Ӧ�Ļ�ѧ����ʽ��Fe+CuSO4=FeSO4+Cu��
�������仯������ϡ���������ⷴӦ�����Ȼ�����ˮ����ȥ����Ļ�ѧ����ʽΪFe2O3+6HCl=2FeCl3+3H2O��
������������������������Ӧ���������������������ӣ���������ϡ���ᷴӦʹ������Ԫ�ؽ���ϡ������Һ�У����������٣�����b��a��c��
�ٽ��������ֱ���뵽����ͭ��Һ��������������ͭ��Ӧ����������������ͭ��Ӧ���ʿ��Լ��𣬹���ȷ���ڽ����ֱ���뵽������������ͭ��Һ�ж���������Ӧ����ֻ��˵��������ã����ܼ�������ͭ���ʴ��۽�ͭ�����ֱ���뵽��������Һ�ж���������Ӧ��ֻ��˵��������ã����ܼ���ͭ�������ʴ��ܽ�ͭ�ֱ���뵽����������������Һ�У�ͭ��������������Ӧ��������������Ӧ���ʿ��Լ��𣬹���ȷ���ݽ�����������ͭ��Һ�У����Է�Ӧ��˵������ͭ���ã���ͭ������������Һ�з�����Ӧ��˵��ͭ�������ã��ʿ��Լ��𣬹���ȷ����ѡ�٢ܢݣ�
��3���ڽ����˳���������Mg![]() Fe
Fe![]() Cu�������Ȼ�ͭ���Ȼ������Ļ����Һ�м���һ������þ�ۣ�þ�����Ȼ�ͭ��Ӧ�����Ȼ�ͭ��Ӧ��ȫ������Ȼ�������Ӧ��ֻ�з�����Ӧ����һ�����Ȼ�þ���ɣ��Ȼ������Ȼ������������п���û�У���һ���е���MgCl2��������ϡ���������ݲ�����˵��������һ��������������þ����������һ�����е�������Cu��Fe��
Cu�������Ȼ�ͭ���Ȼ������Ļ����Һ�м���һ������þ�ۣ�þ�����Ȼ�ͭ��Ӧ�����Ȼ�ͭ��Ӧ��ȫ������Ȼ�������Ӧ��ֻ�з�����Ӧ����һ�����Ȼ�þ���ɣ��Ȼ������Ȼ������������п���û�У���һ���е���MgCl2��������ϡ���������ݲ�����˵��������һ��������������þ����������һ�����е�������Cu��Fe��

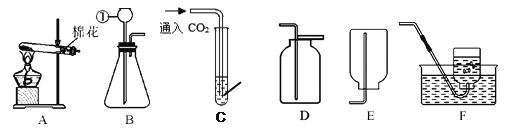
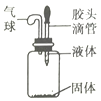
����Ŀ����һ�������ļ����������������������˹�������Һ��������������ҵ�����֮���ϵ��������ͼ���߱�ʾ���ǣ� ��

ѡ�� | �� | �� |
A | ϡ���� | ����������Һ |
B | ϡ���� | ̼��Ʒ�ĩ |
C | ϡ���� | п�� |
D | ��������Һ | ͭ�� |