题目内容
【题目】(8分)某化学小组初步设计了“收集不同体积比例的二氧化碳和一氧化碳混合气体”的实验方案。
方案一:如图1所示
(1)请写出硬质玻璃管中发生反应的化学方程式: 。
(2)该实验能获得二氧化碳和一氧化碳混合气体,其原因是 。
方案二:如图2所示
请写出该气体与炭粉发生反应的化学方程式: .
方案三:如图3所示
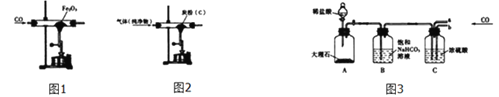
(提示:饱和NaHCO3溶液的作用是除去HCl气体,部分夹持装置及导管已略去)
请回答下列问题:
(1)写出装置A中发生反应的化学方程式: 。
(2)CO气体应由 (填“a”或“b”)通入。
(3)写出装置C中浓硫酸的两点主要作用:
① ;
② 。
【答案】方案一:(1)Fe2O3+3CO![]() 2Fe+3CO2(2)一氧化碳没有完全参与反应,有剩余 方案二:CO2+C
2Fe+3CO2(2)一氧化碳没有完全参与反应,有剩余 方案二:CO2+C![]() 2CO 方案三:(1)CaCO3+2HCl═CaCl2+H2O+CO2↑(2)b(3)①除去二氧化碳中的水蒸气②通过观察导管口的气泡来判断是否得到了混合气体
2CO 方案三:(1)CaCO3+2HCl═CaCl2+H2O+CO2↑(2)b(3)①除去二氧化碳中的水蒸气②通过观察导管口的气泡来判断是否得到了混合气体
【解析】
试题分析:硬质玻璃管中发生反应的化学方程式Fe2O3+3CO![]() 2Fe+3CO2;该实验能获得二氧化碳和一氧化碳混合气体,其原因是一氧化碳没有完全参与反应,有剩余;产生的二氧化碳和碳在高温下反应生成一氧化碳,装置A中发生反应的化学方程式:CaCO3+2HCl═CaCl2+H2O+CO2↑;CO气体应由b端进入,充分和浓硫酸接触,装置C中浓硫酸的两点主要作用:①除去二氧化碳中的水蒸气②通过观察导管口的气泡来判断是否得到了混合气体。
2Fe+3CO2;该实验能获得二氧化碳和一氧化碳混合气体,其原因是一氧化碳没有完全参与反应,有剩余;产生的二氧化碳和碳在高温下反应生成一氧化碳,装置A中发生反应的化学方程式:CaCO3+2HCl═CaCl2+H2O+CO2↑;CO气体应由b端进入,充分和浓硫酸接触,装置C中浓硫酸的两点主要作用:①除去二氧化碳中的水蒸气②通过观察导管口的气泡来判断是否得到了混合气体。

练习册系列答案
 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目