题目内容
(2010?南通模拟)在硬质玻璃管里装有16g氧化铜粉末,通入一氧化碳气体,加热一段时间后冷却,玻璃管内剩余固体的质量为 13.6g.求:剩余固体中含有哪些物质?它们的质量分别是多少?
【答案】分析:根据固体的质量差,利用化学反应方程式来计算反应的氧化碳的质量,进一步确定剩余固体的成分,及它们的质量.
解答:解:设参加反应的氧化铜的质量为x,则.
CuO+CO Cu+CO2 △m
Cu+CO2 △m
80 64 80-64=16
x 16g-13.6g=2.4g
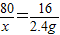 ,
,
解得x=12g,
则16g氧化铜没有完全反应,剩余固体中含剩余的氧化铜和生成的铜,
剩余氧化铜的质量为16g-12g=4g,
生成铜的质量为13.6g-4g=9.6g,
答:剩余固体中含有氧化铜和铜,它们的质量分别为4g、9.6g.
点评:本题考查学生利用差量法和化学反应方程式的计算,学生应明确该反应中固体不一定完全反应,不可将混合物质量直接代入化学方程式计算.
解答:解:设参加反应的氧化铜的质量为x,则.
CuO+CO
 Cu+CO2 △m
Cu+CO2 △m80 64 80-64=16
x 16g-13.6g=2.4g
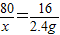 ,
,解得x=12g,
则16g氧化铜没有完全反应,剩余固体中含剩余的氧化铜和生成的铜,
剩余氧化铜的质量为16g-12g=4g,
生成铜的质量为13.6g-4g=9.6g,
答:剩余固体中含有氧化铜和铜,它们的质量分别为4g、9.6g.
点评:本题考查学生利用差量法和化学反应方程式的计算,学生应明确该反应中固体不一定完全反应,不可将混合物质量直接代入化学方程式计算.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

 (2010?南通模拟)小明和小华两同学进行盐酸与镁反应制取氢气的实验研究.小华用较稀的盐酸与镁反应,小明用较浓的盐酸与镁反应.他们分别取等质量的镁与足量盐酸在烧杯中反应,并从反应的开始每隔一段时间测定.烧杯中物质总质量随反应时间的变化情况如图所示.试回答下列问题:
(2010?南通模拟)小明和小华两同学进行盐酸与镁反应制取氢气的实验研究.小华用较稀的盐酸与镁反应,小明用较浓的盐酸与镁反应.他们分别取等质量的镁与足量盐酸在烧杯中反应,并从反应的开始每隔一段时间测定.烧杯中物质总质量随反应时间的变化情况如图所示.试回答下列问题: