题目内容
【题目】核电荷数为1~18的元素的原子结构示意图等信息如图,回答下列问题: 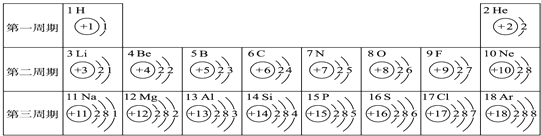
(1)锂原子的核电荷数为 .
(2)16号元素的原子在化学反应中比较容易(填“得”或“失”)电子,该元素属于(填“金属”或“非金属”)元素.
(3)写出表中关于8号元素的一条信息: .
(4)在第三周期中,各原子核外电子排布的变化规律是 .
(5)写出核外电子排布与氖原子相同的阳离子和阴离子符号各一个:阳离子 , 阴离子 .
【答案】
(1)3
(2)得;非金属
(3)原子序数为8等(合理即可)
(4)原子核外电子层数相同(或从左到右,各原子核外电子排布的变化规律是最外层电子数依次增加等,合理即可)
(5)Na+(或Mg2+或Al3+);O2﹣(或F﹣)
【解析】(1)由锂元素周期表中的一格可知,左上角的数字为3,表示原子序数为3;根据原子序数=核电荷数,则锂原子的核电荷数为3;或由锂原子的结构示意图,圆圈内的数字是3,锂原子的核电荷数为3.(2)16号元素的原子,其最外层电子数为6,在化学反应中易得到2个电子而形成阴离子.该元素为硫元素,属于非金属元素.(3)8号元素左上角的数字为8,表示原子序数为8;字母表示该元素的元素符号,其元素符号为O.由8号元素原子的结构示意图,其核内质子数为8,核外由2个电子层,最外层电子数为6等(合理即可).(4)在第三周期中,各原子结构的共同之处是原子核外电子层数相同;该周期中,从左到右,各原子核外电子排布的变化规律是最外层电子数依次增加.(5)氖原子核外有2个电子层,第一层上有2个电子,第二层上有8个电子,钠离子、镁离子、铝离子属于阳离子,氧离子、氟离子属于阴离子,核外电子排布均与氖原子相同;离子符号分别是Na+(或Mg2+或Al3+)、O2﹣(或F﹣).

 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案【题目】某兴趣小组欲通过实验证明“二氧化锰是氯酸钾受热分解的催化剂”这一命题,他设计并完成了下表所示的探究实验
(1)请填写上表中未填完的空格;
实验操作 | 实验现象 | 实验结论或总结 | ||
各步骤结论 | 总结 | |||
实验一 | 将氯酸钾加热至融化,伸入带火星的木条 | 木条复燃 | 氯酸钾受热分解能产生氧气,但是 | 二氧化锰是氯酸钾受热分解的催化剂 |
实验二 | 加热二氧化锰,伸入带火星的木条, | 木条不复燃 | 二氧化锰受热不产生氧气. | |
实验三 | 木条迅速复 燃 | 二氧化锰能加快氯酸钾的分解速度. |
(2)在探究实验中,“实验一”和“实验二”起的作用是 ;
(3)小英同学认为仅由上述实验还不能完全得出表内“总结”,她补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明.
第一方面的实验操作中包含了两次称量,其目的是 ;第二方面的实验是要验证回收的二氧化锰是否还有 作用.
(4)写出此反应的文字表达式 .
