��Ŀ����
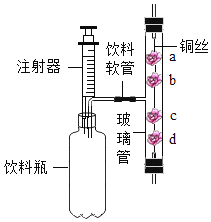
����Ŀ���߽�ʵ���ң���ʹ�����ڶ��ֲ��������鵽ѧϰ�Ŀ��֡�ij��ѧ��ȤС���ͬѧ������40g��������Ϊ5%���Ȼ�����Һ��ȫ������������ͼ��ʾ��

��ش��������⣺
(1)����ʱ��Ӧ��ȡ_____gʳ�Σ���ˮ���ܶȽ��Ƶؿ���1g/mL�������10mL��50mL��100mL����Ͳ�����ѡȡ_____mL����Ͳ��
(2)ʵ����ʹ�ò�������Ŀ����_____��
(3)�������õ���Һ���ʵ�����������С��5%�����ܵ�ԭ����_____(дһ��)��
���𰸡�2 50 �����ܽ� ��ȡˮ�����ʱ���Ӷ���
��������
(1)����ʱ��Ӧ��ȡʳ������Ϊ��40g��5%��2g����Ҫˮ�����Ϊ��(40g��2g)��1g/mL��38mL�������10mL��50mL��100mL����Ͳ�����ѡȡ50mL����Ͳ�����2��50��
(2)ʵ����ʹ�ò�������Ŀ���Ǽ����ܽ⡣��������ܽ⡣
(3)�������õ���Һ���ʵ�����������С��5%�����ܵ�ԭ������ȡˮ�����ʱ���Ӷ�����ת���Ȼ������ձ��й���������һ���ֵȡ������ȡˮ�����ʱ���Ӷ�����

 ��У����ϵ�д�
��У����ϵ�д�����Ŀ��ijʵ��С�����ⶨһƿBa(NO3)2��Һ������������ȡ100g Ba(NO3)2��Һ������������Na2SO4��Һ��������Һ���������ɳ���������ϵ���±���
���� | 1 | 2 | 3 | 4 | 5 |
����Na2SO4��Һ����/g | 20 | 40 | 60 | 80 | 100 |
���ɳ�������/g | 2.33 | 4.66 | m | 9.32 | 9.32 |
��1��������m����ֵΪ_____��
��2������Na2SO4��Һ��ԭBa(NO3)2��Һ������Ϊ_____ʱǡ����ȫ��Ӧ��
��3������ԭBa(NO3)2��Һ���ʵ�����������_____
����Ŀ����ʯ����CaO��NaOH�Ĺ������ͨ����������CO2���������塣ijѧУС����ʵ����ȡ��һ�������Ѿ�ʹ�ù��ļ�ʯ����Ʒ��������ɷֽ���������̽����
��������룩�ü�ʯ����Ʒ�п��ܺ���CaO��________(�ѧʽ)��CaCO3��NaOH��NaCO3��
����Ʒ�����(1)��ͬѧ���ձ��з��������ĸü�ʯ����Ʒ��������������ˮ��ֽ��裬���ã��а�ɫ�������֣���ͬѧ��Ϊ��Ʒ��һ������CaCO3������Ϊ��ͬѧ�Ľ����Ƿ��Ͻ���
�����ǣ�_____________
(2)��ͬѧ��һ�����ʵ�鲢������֤���������£�
ʵ����� | ʵ������ | ʵ����� |
�ٴӼ�ͬѧ���ձ���ȡ�����ϲ���Һ���Թ��У������еμ�����______��Һ�� | �а�ɫ�������� | ��Ʒ��һ����NaCO3�� |
�ڽ����������õ��Ļ������ˣ�����Һ�еμ���ɫ��̪��Һ�� | ���������� | ��Һ�в����У�____�� |
��ʵ����ۣ�����Ϊͨ�����ϼס�����λͬѧ��ʵ��̽�����Ƿ����ȷ���ü�ʯ����Ʒ����ɳɷ֣����ܣ���д������ɣ������ܣ���˵�����ɡ�______________

��ʵ�鷴˼����ͬѧ��һ�����������ͼ��ʾ��ʵ��װ�ã�ͨ������Bװ�õ������仯���ⶨһ������Ʒ������ϡ���ᷴӦ�����ɵ�CO2������(���������ã�ÿ������ȫ��Ӧ����������)������ͬѧ���ղ�õ�CO2������ʵ��ֵС������Ϊ����ԭ���ǣ�___________
����Ŀ����ѧ������������أ��������̺��ŷḻ�Ļ�ѧ֪ʶ��
(1)������һ����ζ��Ӫ����ʳƷ��������ԭ����Ҫ�У���������ۡ���ɰ�ǡ�ţ�̡�����͵ȣ����и���������а�ɰ�Ǻ�_________��
(2)�����е�������ϴ��һ��Ҫ���ɷ��ã����Լ���_______������ʴ��Ӱ�졣
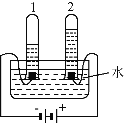
(3)��ˮ��������Ҫ��������ͼ��ʾ��
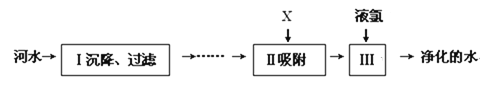
��������������X�Լ�������__________����___________�����жϾ�����ˮ��Ӳˮ������ˮ��
(4)��ͥ���õļ�����������Ҫ�ɷ����£�
���õ����� | ������ | ȥ�۷� | �ܵ�ͨ |
��Ҫ�ɷ� | ���� | ̼���� | �������ơ����� |
���������ܳ�ˮ��Ҳ��ȥ���⣬��д��������ȥ����ķ�Ӧ����ʽ___________________.
��ȥ�۷�����������ܻ��ʹ�ã���ԭ����________________(�û�ѧ����ʽ��ʾ)���۹ܵ�ͨʹ��ʱ���ܽӴ�Ƥ����ԭ����___________��ʹ��ʱAl��NaOH��Һ��Ӧ�ų��������ȣ��ɼӿ�NaOH���ٻ�������á��ڷ�Ӧ����NaAlO2�У���Ԫ�صĻ��ϼ�Ϊ___�ۡ�
(5)��ͼ��ȼ����ˮ��ʾ��ͼ�����ݴ�ͼ�ش�
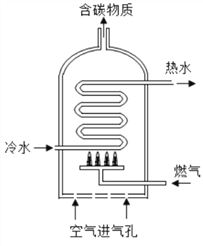
��ij��ˮ����������Ϊȼ����д������ȫȼ�յĻ�ѧ����ʽ___________.
���������������������ֶ���ʱ��ȼ�ս������ж�����M��M�Ļ�ѧʽΪ__________��