题目内容
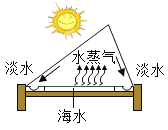
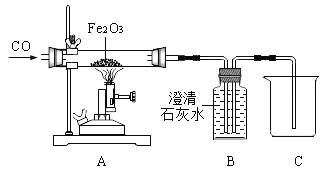
【题目】氮气在高温、高能量条件下可与某些物质发生反应。如图是以空气和必要的原料合成氮肥(NH4NO3)的工业流程。请按要求回答下列问题:
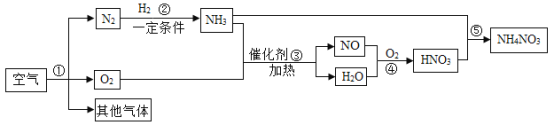
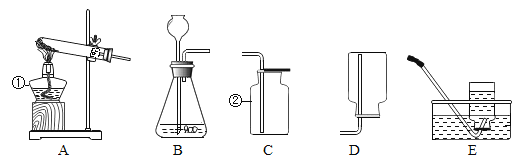
(1)步骤①是利用各物质的_____(填“熔点”或“沸点”)不同进行分离。
(2)写出步骤③中发生反应的化学方程式____,该反应中使用了催化剂,反应前后,催化剂的___没有发生改变。
(3)如图是化肥硝酸铵包装袋上的部分说明,由此推测硝酸铵具有的性质是_____(写出一点即可)。

(4)施用该肥料时,要避免与碱性物质混合使用,原因是________。
【答案】沸点 4NH3+5O2 4NO+6H2O 质量和化学性质 易溶于水,受热易分解 产生氨气,降低肥效
4NO+6H2O 质量和化学性质 易溶于水,受热易分解 产生氨气,降低肥效
【解析】
(1)分离液态空气是利用空气中各物质沸点不同,分离各物质,故填:沸点。
(2)步骤3氨气和氧气在催化剂和加热条件下生成了一氧化氮和水,化学方程式为4NH3+5O2 4NO+6H2O,催化剂可以改变反应速率,质量和化学性质在反应前后不变,故填:4NH3+5O2
4NO+6H2O,催化剂可以改变反应速率,质量和化学性质在反应前后不变,故填:4NH3+5O2 4NO+6H2O;质量和化学性质。
4NO+6H2O;质量和化学性质。
(3)硝酸铵需防潮防嗮,密封保存,据此推测硝酸铵具有的性质是溶于水,受热易分解,故填:溶于水,受热易分解。
(4)施用硝酸铵时,要避免与碱性物质混合使用,原因硝酸铵和碱性物质在一起会生成氨气 ,降低肥效,故填:产生氨气,降低肥效。

【题目】研究可燃物燃烧的条件。
已知:酒精灯火焰的温度约为500℃,一些物质的着火点如下表所示。
物质 | 红磷 | 木材 | 无烟煤 |
着火点/℃ | 240 | 250~330 | 700~750 |
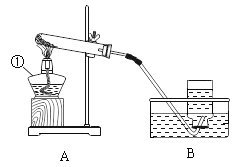
(1)实验1:在铜片两端分别放置木块和无烟煤块,点燃酒精灯加热一段时间,能说明可燃物燃烧需要温度达到着火点的实验现象是_____。
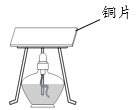
(2)实验2:将红磷置于铜片上,用沙土覆盖,点燃酒精灯持续加热,红磷始终不燃烧,其原因是_____。