题目内容
【题目】在一烧杯中盛有22.3gNa2CO3和NaCl组成的固体混合物,向其中逐渐滴加溶质质量分数为10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示:请根据题意回答问题:
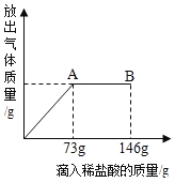
(1)当滴加了73g稀盐酸时,放出气体的总质量为 g
(2)当滴加稀盐酸至图中B点时,烧杯中溶液里的溶质是 (写化学式).
(3)当滴加了73g稀盐酸时(即A点时),烧杯中为不饱和溶液,试通过计算求出其中溶质的质量分数.(计算结果保留一位小数
【答案】(1)4.4(1分) (2)NaCl 、HCl(1分)
(3)25.7%(6分)
【解析】
试题分析:由题可知反应的氯化氢的质量为73g×10%=7.3g;当滴加稀盐酸至图中B点时,盐酸过量烧杯中溶液里的溶质是氯化钠和氯化氢;设当滴加了73g稀盐酸时生成氯化钠的质量为x,碳酸钠的质量为y,则:
Na2CO3+2HCl====2NaCl+H20+CO2↑
106 73 117 44
y 7.3g X z
73/117=7.3g/x x= 11.7g
106/73=y/7.3g y=10.6g
73/7.3g=44/z z=4.4g
当滴加了73g稀盐酸时所得溶液中溶质的质量分数为
(11.7g+22.3g-10.6g )÷(22.3g+73g-4.4g)×100%=25.7%

练习册系列答案
相关题目