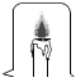
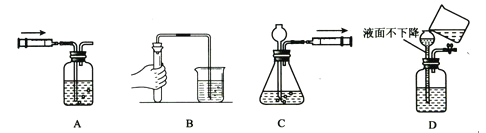
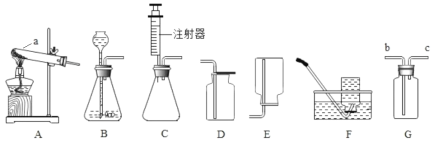
题目内容
【题目】A﹣I为初中所学的物质,A为生石灰,C为大理石的主要成分,D为蓝色沉淀,E为硫酸亚铁溶液,图中“→”表示物质间存在相互转化的关系(各步反应均恰好完全,部分生成物末标出),根据如图回答问题:
(1)B的化学式是_____;H的化学式是_____;
(2)由B→C的化学方程式为_____;
(3)G→E的化学方程式为_____。
【答案】Ca(OH)2,Fe;Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;Fe+CuSO4=FeSO4+Cu。
【解析】
推断题往往以框图的形式出现,解答此类题,首先要认真审题,找出该题的突破口。
A为生石灰,则A是氧化钙,CaO+H2O==Ca(OH)2 ,所以B是Ca(OH)2 ,C为大理石的主要成分,C是CaCO3。Na2CO3 + Ca(OH)2 == CaCO3↓+ 2NaOH,则I是Na2CO3,D为蓝色沉淀,D是 Cu(OH)2,E为硫酸亚铁溶液,由于Fe+CuSO4 ==Cu+FeSO4 ,则G是CuSO4,H是Fe,F是Cu。(1)B的化学式是Ca(OH)2;H的化学式是Fe;(2)B→C的化学方程式为: Ca(OH)2+Na2CO3=CaCO3↓+2NaOH(3)G→E的化学方程式为:Fe+CuSO4=FeSO4+Cu

【题目】某实验小组的同学为了测定实验室中氯酸钾(KClO3)样品的纯度,取一定量该样品与1g二氧化锰混合,其总质量为6g,依次加热该混合物T1、T2、T3、T4时间后,分别冷却称量剩余固体质量,记录的有关数据如表
(样品中的杂质不参与化学反应:有关方程式: 2KClO3 ![]() 2KCl+3O2↑)
2KCl+3O2↑)
加热时间 | T1 | T2 | T3 | T4 |
剩余固体质量/g | 4.24 | 4.16 | 4.08 | 4.08 |
(1)氯酸钾中钾、氯、氧元素的质量比为______;
(2)完全反应后产生氧气的总质量为______;
(3)计算氯酸钾样品中氯酸钾的质量分数_______.(写出计算过程)