题目内容
【题目】将一定质量的Zn加入到![]() 、
、![]() 、
、![]() 三种物质的混合溶液中,充分反应后过滤,滤液为无色,则下列判断正确的是( )
三种物质的混合溶液中,充分反应后过滤,滤液为无色,则下列判断正确的是( )
A.滤渣一定含有Ag、Cu
B.向滤液中滴加稀盐酸,一定产生白色沉淀
C.滤液中最多含有三种溶质
D.反应前后金属固体的质量一定变大
【答案】A
【解析】
镁比锌活泼,锌比铜活泼,铜比银活泼,将一定质量的Zn加入到Mg(NO3)2、Cu(NO3)2、AgNO3三种物质的混合溶液中,锌不能和硝酸镁反应,先和硝酸银反应生成硝酸锌和银,等硝酸银完全后,再和硝酸铜反应生成硝酸锌和铜。
根据以上分析可知:
A、充分反应后过滤,滤液为无色,说明硝酸银、硝酸铜已经完全反应,因此滤渣一定含有Ag、Cu,故A正确;
B、滤液中不存在硝酸银,向滤液中滴加稀盐酸,不能产生白色沉淀,故B错误;
C、滤液中含有两种溶质,即硝酸镁、硝酸锌,故C 错误;
D、锌和硝酸银反应生成硝酸锌和银,化学方程式为:2AgNO3+Zn=Zn(NO3)2+2Ag,每65份质量的锌能生成216份质量的银,反应后固体质量增大;锌和硝酸铜反应生成硝酸锌和铜,化学方程式为:Cu(NO3)2+Zn=Zn(NO3)2+Cu,每65份质量的锌能生成64份质量的铜,反应后固体质量减小,因此反应后金属固体的质量可能增大,也可能减小,故D错误。故选A。

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
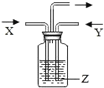
【题目】如图,将气体 X 和气体 Y 同时通入液体 Z 中,最终一定能看到液体变浑浊的是( )
X | Y | Z | 装置 | |
A | H2 | N2 | 水 |
|
B | HCl | CO2 | 澄清石灰水 | |
C | O2 | HCl | 硝酸银溶液 | |
D | O2 | CO2 | 烧碱溶液 |
A. AB. BC. CD. D