题目内容
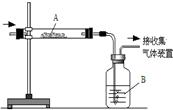 右图所示是初中化学中常用的实验装置,它具有多种用途,可用于探究或验证气体的性质、除杂质、转化物质等.现用该装置完成下列有关实验:
右图所示是初中化学中常用的实验装置,它具有多种用途,可用于探究或验证气体的性质、除杂质、转化物质等.现用该装置完成下列有关实验:(1)若除去CO2中少量CO,则A中盛放的药品是
氧化铜
氧化铜
,需要增加的仪器是酒精灯
酒精灯
.(2)若探究CO2能与C反应生成CO,则只要在A中放一定量的碳粉,然后在B的出口处
放置一个点燃的酒精灯
放置一个点燃的酒精灯
,若出现气体燃烧
气体燃烧
现象,就证明能生成CO,B中溶液的作用是除去未反应的二氧化碳
除去未反应的二氧化碳
.(3)若用上述实验装置测定水中氢、氧元素的质量比(反应原理是H2+CuOCu+H2O,通过A中减轻的质量,得到生成的水中氧元素的质量),A中放氧化铜,则B中所选用的药品是
浓硫酸
浓硫酸
,还需要测定或记录的数据是称量并记录反应前后A、B两处仪器的质量
称量并记录反应前后A、B两处仪器的质量
.分析:(1)根据CO在高温下和氧化铜反应,转化为二氧化碳进行解答.
(2)根据二氧化碳不能燃烧,若生成的气体燃烧则可证明CO生成.
(3)氢气还原氧化铜生成水,用B吸收水分,水中氢元素来之氢气,氧元素来之氧化铜,A中固体质量的变化即为氧的质量,而B质量的变化为水的质量,由此可求氢氧元素的质量比.
(2)根据二氧化碳不能燃烧,若生成的气体燃烧则可证明CO生成.
(3)氢气还原氧化铜生成水,用B吸收水分,水中氢元素来之氢气,氧元素来之氧化铜,A中固体质量的变化即为氧的质量,而B质量的变化为水的质量,由此可求氢氧元素的质量比.
解答:解:(1)除二氧化碳中的一氧化碳,可通过灼热的氧化铜,一氧化碳被氧化成二氧化碳,反应装置中缺少加热装置.
故答案为:氧化铜;酒精灯
(2)二氧化碳在高温下和碳粉反生成一氧化碳,因为二氧化碳不能燃烧,所以只要证明除去二氧化碳气体后剩余的气体可以燃烧,即可证明有CO生成.
故答案为:放置一个点燃的酒精灯;气体燃烧;除去未反应的二氧化碳
(3)氢气可以还原氧化铜生成水,浓硫酸具有吸水性,能吸收水分,氧化铜反应后质量减轻,减少的即为氧元素质量,浓硫酸质量增加,增加的为水的质量,减去氧元素质量即为氢元素质量,由此可求氢氧元素的质量比,
故答案为:浓H2SO4;称量并记录反应前后A、B两处仪器的质量
故答案为:氧化铜;酒精灯
(2)二氧化碳在高温下和碳粉反生成一氧化碳,因为二氧化碳不能燃烧,所以只要证明除去二氧化碳气体后剩余的气体可以燃烧,即可证明有CO生成.
故答案为:放置一个点燃的酒精灯;气体燃烧;除去未反应的二氧化碳
(3)氢气可以还原氧化铜生成水,浓硫酸具有吸水性,能吸收水分,氧化铜反应后质量减轻,减少的即为氧元素质量,浓硫酸质量增加,增加的为水的质量,减去氧元素质量即为氢元素质量,由此可求氢氧元素的质量比,
故答案为:浓H2SO4;称量并记录反应前后A、B两处仪器的质量
点评:本题考查了二氧化碳和一氧化碳的化学性质,氢气还原氧化铜的原理,最后的实验设计题对学生要求很高.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
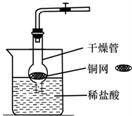 27、CO2是初中化学重点研究的气体之一.某化学兴趣小组设计了如下实验来探究CO2的制取和性质:
27、CO2是初中化学重点研究的气体之一.某化学兴趣小组设计了如下实验来探究CO2的制取和性质: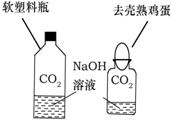
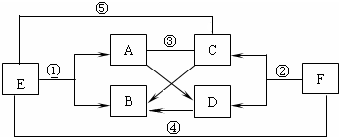 (2009?昌平区二模)A、B、C、D、E、F是初中化学常见的六种化合物,其中B由两种元素组成,且元素质量比为1:8,它们之间的转化关系如右图所示(图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,图中已略去部分物质).试回答以下问题
(2009?昌平区二模)A、B、C、D、E、F是初中化学常见的六种化合物,其中B由两种元素组成,且元素质量比为1:8,它们之间的转化关系如右图所示(图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,图中已略去部分物质).试回答以下问题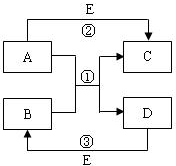 A、B、C、D、E是初中化学中常见的物质,其转化关系如右图所示(产物中的某些物质可能略去).请依据转化关系图,写出符合要求的一组答案.
A、B、C、D、E是初中化学中常见的物质,其转化关系如右图所示(产物中的某些物质可能略去).请依据转化关系图,写出符合要求的一组答案.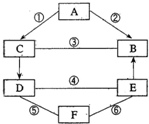 A、B、C、D、E、F都是初中化学常见的物质,其中B是植物进行光合作用的一种重要原料.它们之间的关系如右图所示.(图中“一”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,有关反应条件和其他物质已略去.)
A、B、C、D、E、F都是初中化学常见的物质,其中B是植物进行光合作用的一种重要原料.它们之间的关系如右图所示.(图中“一”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,有关反应条件和其他物质已略去.)