题目内容
 (1)试配平下列化学方程式:
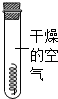
(1)试配平下列化学方程式:(2)试验时对铜丝加热利用热传导使下方白磷燃烧,待试管冷却后
打开弹簧夹,此时可观察到的现象为
(3)如果装置气密性不好,则测出的O2与N2的体积比将
考点:空气组成的测定,化学方程式的配平
专题:空气与水
分析:(1)根据质量守恒定律反应前后原子的种类和个数都不变配平;
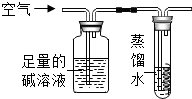
(2)根据空气中氧气约占其体积的五分之一,磷燃烧生成了五氧化二磷,消耗氧气,使集气瓶内压强减小,水被倒吸入集气瓶,得出氧气和氮气的体积比;
(3)根据若装置漏气,则倒吸的水量减少甚至不会倒吸分析.
(2)根据空气中氧气约占其体积的五分之一,磷燃烧生成了五氧化二磷,消耗氧气,使集气瓶内压强减小,水被倒吸入集气瓶,得出氧气和氮气的体积比;
(3)根据若装置漏气,则倒吸的水量减少甚至不会倒吸分析.
解答:解:(1)采用最小公倍数法配平,选“O”为起点元素,最小公倍数为10,因此氧气前为5,五氧化二磷前为2,观察磷原子的个数是4,故答案为:4;5;2;
(2)空气中氧气约占其体积的五分之一,磷燃烧消耗氧气使集气瓶内压强减小,待试管冷却后打开弹簧夹,此时可观察到的现象为水被吸入集气瓶约占集气瓶容积的
,剩下的
主要是氮气,从而证明空气中氧气和氮气的体积比为 1:4;故答案为:水被吸入集气瓶约占集气瓶容积的
;1:4;
(3)若装置漏气,导致空气进入集气瓶内,因此测得的氧气的体积分数小于五分之一,则测出的O2与N2的体积比将偏小;故答案为:偏小.
(2)空气中氧气约占其体积的五分之一,磷燃烧消耗氧气使集气瓶内压强减小,待试管冷却后打开弹簧夹,此时可观察到的现象为水被吸入集气瓶约占集气瓶容积的
| 1 |
| 5 |
| 4 |
| 5 |
| 1 |
| 5 |
(3)若装置漏气,导致空气进入集气瓶内,因此测得的氧气的体积分数小于五分之一,则测出的O2与N2的体积比将偏小;故答案为:偏小.
点评:本题考查了空气中氧气含量的测定,探究测定空气中氧气含量的误差分析,解答此类试题时,可以从药品的用量、装置的气密性以及装置是否冷却等方面分析解答即可.

练习册系列答案
相关题目
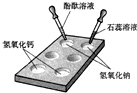 如图为某学习小组在白色点滴板上进行的有关“碱的化学性质”的探究实验.使用白色点滴板进行实验的优点是
如图为某学习小组在白色点滴板上进行的有关“碱的化学性质”的探究实验.使用白色点滴板进行实验的优点是