题目内容
【题目】向一定质量的Na2CO3、Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示,下列说法正确到是( ) 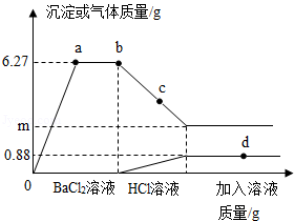
A.0﹣a段发生了一个反应
B.c点沉淀的成分为一种
C.取d点对应的溶液,滴加硝酸银溶液,有白色沉淀,说明加入的盐酸已过量
D.m=2.33
【答案】D
【解析】解:A、0﹣a段发生了2个反应,即氯化钡和碳酸钠反应生成碳酸钡沉淀和氯化钠,和硫酸钠反应生成硫酸钡沉淀和氯化钠,该选项说法不正确; B、c点沉淀的成分为2种,即硫酸钡和没有反应的碳酸钡,该选项说法不正确;
C、取d点对应的溶液,滴加硝酸银溶液,有白色沉淀,不能说明加入的盐酸已过量,这是因为稀盐酸和碳酸钡反应生成的氯化钡能和硝酸银反应生成白色沉淀氯化银,该选项说法不正确;
D、设碳酸钡质量为x,
BaCO3+2HCl═BaCl2+H2O+ | CO2↑ |
197 | 44 |
x | 0.88g |
![]() =
= ![]() ,
,
x=3.94g,
则m=6.27﹣3.94=2.33,
该选项说法正确.
故选:D.
氯化钡和碳酸钠反应生成碳酸钡沉淀和氯化钠,和硫酸钠反应生成硫酸钡沉淀和氯化钠,稀盐酸能和碳酸钡反应生成氯化钡、水和二氧化碳,硫酸钡不能和稀盐酸反应.

练习册系列答案
相关题目