题目内容
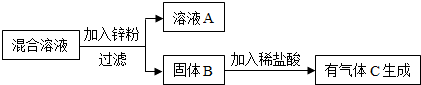
某化学小组用一定量AgNO3和Cu(NO3)2混合溶液进行了如图实验,并对溶液A和固体B的成分进行了分析和实验探究.下列说法中不正确的是( )

| A、溶液A中一定存在Zn(NO3)2 |
| B、溶液A中可能存在Cu(NO3)2 |
| C、实验说明加入的锌粉是过量的 |
| D、实验中所涉及的反应均属于置换反应 |
考点:金属的化学性质,置换反应及其应用
专题:金属与金属材料
分析:根据金属活动性顺序及其运用分析.排在氢之前的金属可与稀盐酸或稀硫酸反应产生氢气,排在前面的金属(除钾、钙、钠外)可将排在后面的金属从其盐溶液中置换出来.故AgNO3和Cu(NO3)2都会与锌粉反应,而铜与硝酸银溶液反应、锌与稀盐酸反应.
解答:解:根据金属活动性顺序:Zn>(H)>Cu>Ag,故可推测:
A、AgNO3和Cu(NO3)2都会与锌粉反应,则溶液A中一定存在Zn(NO3)2,故正确;
B、因向固体B加盐酸有气体生成,所以固体B中一定有锌,故固体B为Ag、Cu和Zn,则实验说明加入的锌粉是过量的,则溶液A中不可能存在Cu(NO3)2;故错误;
C、因向固体B加盐酸有气体生成,所以固体B中一定有锌,故固体B为Ag、Cu和Zn,则实验说明加入的锌粉是过量的,故正确;
D、实验中锌与AgNO3和Cu(NO3)2反应;铜与硝酸银溶液反应、锌与稀盐酸反应,均属于置换反应.故正确.
故选:B.
A、AgNO3和Cu(NO3)2都会与锌粉反应,则溶液A中一定存在Zn(NO3)2,故正确;
B、因向固体B加盐酸有气体生成,所以固体B中一定有锌,故固体B为Ag、Cu和Zn,则实验说明加入的锌粉是过量的,则溶液A中不可能存在Cu(NO3)2;故错误;
C、因向固体B加盐酸有气体生成,所以固体B中一定有锌,故固体B为Ag、Cu和Zn,则实验说明加入的锌粉是过量的,故正确;
D、实验中锌与AgNO3和Cu(NO3)2反应;铜与硝酸银溶液反应、锌与稀盐酸反应,均属于置换反应.故正确.
故选:B.
点评:本题难度不是很大,主要考查了对金属活动性顺序的应用和理解,培养学生的应用能力和解决问题的能力.

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
化学反应可以为人类提供能量,下列反应中能量变化不明显的是( )
| A、火药爆炸 |
| B、生石灰与水反应 |
| C、二氧化碳与水反应 |
| D、木炭在空气中燃烧 |
下列说法不正确的是( )
| A、如果不慎将碱液沾到皮肤上,应立即涂上盐酸溶液 |
| B、在滴有石蕊溶液的水中通入CO2后溶液变红,说明CO2与水反应生成了酸 |
| C、酚酞和NaOH混合溶液中加稀硫酸红色褪去,说明硫酸与氢氧化钠发生了反应 |
| D、熟石灰涂在墙体表面后变硬,原因是熟石灰与CO2反应生成了坚硬的碳酸钙 |
为全球地表温度提高到目前适合人类居住的15℃做出突出贡献的是( )
| A、温室效应 | B、白色污染 |
| C、酸雨腐蚀 | D、臭氧空洞 |
从化学角度看,下列说法正确的是( )
| A、煤炉上放一壶水就能防止一氧化碳中毒 |
| B、发现燃气(天然气、煤气或液化石油气等)泄漏,点火检查泄漏处 |
| C、人类未来最理想的清洁能源是氢气和太阳能 |
| D、常用钢丝球擦洗铝壶可以使其光亮洁净和更耐用 |
下列关于氧气的说法中,错误的是( )
| A、工业上可以利用分离液态空气法制氧气,这一过程是物理变化 |
| B、氧气可以支持燃烧,说明氧气具有可燃性 |
| C、氧气供给呼吸,它和体内物质反应,释放能量,维持生命活动 |
| D、鱼类在水中生存说明水中溶解了一定量的氧气 |
下列关于分子、原子和离子的说法正确的是( )
| A、原子可以转化成离子,离子不能转化成原子 |
| B、化学变化中,分子可以再分,原子不能再分 |
| C、物质的三态主要是分子大小发生变化 |
| D、物质都是由质子、中子、电子构成的 |
化学实验是进行科学探究的重要途径.下列实验操作中,不符合操作规范的是( )
| A、实验室制取气体前要先检查装置的气密性 |
| B、测定溶液的酸碱度,将pH试纸直接伸入待测液中 |
| C、浓硫酸不慎沾到手上,立即用大量的水冲洗,然后涂上3%-5%碳酸氢钠溶液 |
| D、点燃氢气前,一定要先检验氢气的纯度 |
 如图为某品牌矿泉水的部分商标.请阅读商标,回答下列问题
如图为某品牌矿泉水的部分商标.请阅读商标,回答下列问题