题目内容
【题目】小明同学欲通过实验证明“二氧化锰是氯酸钾受热分解的催化剂”这一命题.他设计并完成了下表所示的探究实验:
实验操作 | 实验现象 | 实验结论或总结 | ||
各步骤结论 | 总结 | |||
实验一 | 将氯酸钾加热至熔化,伸入带火星的木条 | 木条复燃 | 氯酸钾受热分解产生氧气,但是 . | 二氧化锰是氯酸钾受热分解的催化剂 |
实验二 | 加热二氧化锰,伸入带火星的木条 | 木条不复燃 | 二氧化锰受热不产生氧气. | |
实验三 | 木条迅速复燃 | 二氧化锰能加快氯酸钾分解,反应的符号表达式为: . | ||
(1)请你帮小明同学填写上表中未填完的空格;
(2)在小明的探究实验中,实验一和实验二起的作用是;
(3)小英同学认为仅由上述实验还不能完全得出表内“总结”,她补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明.
第一方面的实验操作中包含了两次称量,其目的是:;
第二方面的实验是利用“实验三”反应后剩余物,经洗涤、过滤分离出的物质继续实验,接下来的实验操作是 .
【答案】
(1)
时间较长、温度较高;将MnO2与KClO3的混合物加热;2KClO3 ![]() 2KCl+3O2↑
2KCl+3O2↑
(2)对比
(3)比较MnO2在KClO3分解前后的质量;验证从反应后的剩余物中分离出的物质是否能加快KClO3的分解
【解析】解:(1)实验三要看二氧化锰在氯酸钾分解反应中的作用,所以要加热二者的混合物;只加热氯酸钾,要加热到熔化才有少量氧气放出,生成氧气的速率较慢,反应方程式为2KClO3 ![]() 2KCl+3O2↑.(2)实验一和实验二是对比实验,通过对比得出二氧化锰的作用.(3)催化剂的特点是“一变,两不变”,即反应速率变,质量和化学性质不变,要证明物质是催化剂,必须同时验证这三点,所以第一方面:比较MnO2在KClO3分解前后的质量;第二方面:验证从反应后的剩余物中分离出的物质是否能加快KClO3的分解.所以答案是:(1)
2KCl+3O2↑.(2)实验一和实验二是对比实验,通过对比得出二氧化锰的作用.(3)催化剂的特点是“一变,两不变”,即反应速率变,质量和化学性质不变,要证明物质是催化剂,必须同时验证这三点,所以第一方面:比较MnO2在KClO3分解前后的质量;第二方面:验证从反应后的剩余物中分离出的物质是否能加快KClO3的分解.所以答案是:(1)
实验一 | 时间较长、温度较高 | ||
实验三 | 将MnO2与KClO3的混合物加热 | 2KClO3 |
2)对比(或比照等);(3)比较MnO2在KClO3分解前后的质量;验证从反应后的剩余物中分离出的物质是否能加快KClO3的分解.
【考点精析】关于本题考查的催化剂的特点与催化作用和书写化学方程式、文字表达式、电离方程式,需要了解催化剂(触媒):在化学反应中能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质.(一变两不变)催化剂在化学反应中所起的作用叫催化作用;注意:a、配平 b、条件 c、箭号才能得出正确答案.

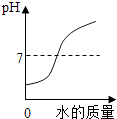
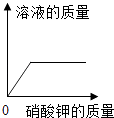
【题目】下列四个图象中,能正确表示对反应变化关系的是( )
|
|
|
|
A.向一定量稀盐酸中加水稀释 | B.一定温度下,向不饱和硝酸钾溶液中加入硝酸钾 | C.加热一定量的高锰酸钾固体 | D.向盐酸和氯化镁的混合溶液中加氢氧化钾溶液 |
A.A
B.B
C.C
D.D
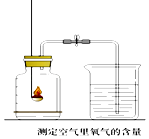
【题目】实验是科学探究的重要方法,如图是测定空气中氧气含量实验的两套装置图,请结合图示回答有关问题. 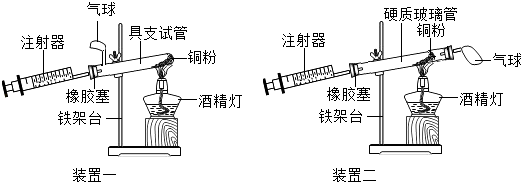
(1)根据下表提供的实验数据,完成下表.
硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
25mL | 15mL | 9mL |
(2)装置一和装置二中气球的位置不同,(填“装置一”或“装置二”)更合理,理由是 .
(3)若实验测得的结果偏小(氧气的体积分数小于21%),可能的原因有哪些?(列举两条)、 .