��Ŀ����
����Ŀ����ѧ�������ǵ����ߣ��������ǵ�����ϢϢ��أ�������ijУ����ͬѧ�ռ���һЩ��־����ǩ����װ��ʵ��ʾ��ͼ����ͼ��ʾ����
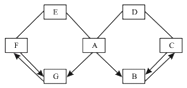
��1��ͼA��ij��ʳ�εİ�װ�����ӵ⺣���еġ��⡱��ָ�����ԭ�ӡ��������ӡ��������ӡ���Ԫ�ء��������û�ѧ������ȷ��ʾ������е�Ԫ�صĻ��ϼ������������мء���Ԫ�ص�������Ϊ �� 
��2��ͼB��ijƷ�ƿ�Ȫˮ�ı�ǩ������ٵ���������ӵķ���Ӧ���� �� ������̪��Һ�������Ȼ��Ȫˮ��Ʒ�У�����ɫ������Ȼ��Ȫˮ�к��ж������ʣ�������һ�����ʿ���������θ�����֢���û�ѧ����ʽ��ʾ�䷴Ӧԭ�� �� 
��3������H��C��O��N��K��Ca���ֳ�����Ԫ�أ���ѡ�����е�Ԫ��д����������Ҫ������ʸ�һ�֣��û�ѧʽ��ʾ�����ٿ������Ϸ��ϵ���������ˮ����ʹ��ɫʯ����Һ���ɫ���������ۿ����������ϵļ�����������ʻԱ����ǰ��ֹ���õ����� ��
���𰸡�
��1��Ԫ�أ� ![]() ��13��16
��13��16
��2��SO42�����죻NaHCO3+HCl=NaCl+H2O+CO2��
��3��KNO3��H2CO3��Ca��OH��2��C2H5OH
���������⣺��1�����ʵ���ɳ���Ԫ�����������ӵ⺣���еġ��⡱��ָ��Ԫ�أ�������е�Ԫ�صĻ��ϼ�Ϊ+5�ۣ�������صĻ�ѧʽ�е�Ԫ�ط��ŵ����Ϸ������+5��������Ϊ�� ![]() �������KIO3�м�Ԫ�ء���Ԫ�ص�������=39����16��3��=39��48=13��16����2����������ӵķ���Ӧ��������������ŵ����ϽDZ����2��������Ϊ��SO42�������ڸÿ�Ȫˮ��pH����7���������ԣ�������̪��Һ����ÿ�Ȫˮ��Ʒ�У����Ժ�ɫ������Ȼ��Ȫˮ�к��ж������ʣ�������һ������̼�����ƿ���������θ�����֢���䷴Ӧԭ���ǣ�NaHCO3+HCl=NaCl+H2O+CO2������3���������ʵ����ʺ���;��ϸ�����Ԫ�ؿ�֪���ٿ������Ϸ��ϵ���������أ���ѧʽ�ǣ�KNO3������ˮ����ʹ��ɫʯ����Һ����������̼�ᣮ��ѧʽ�ǣ�H2CO3���ۿ����������ϵļ����������ƣ���ѧʽ�ǣ�Ca��OH��2����������ʻԱ����ǰ��ֹ���õ������Ǿƾ�����ѧʽ�ǣ�C2H5OH��
�������KIO3�м�Ԫ�ء���Ԫ�ص�������=39����16��3��=39��48=13��16����2����������ӵķ���Ӧ��������������ŵ����ϽDZ����2��������Ϊ��SO42�������ڸÿ�Ȫˮ��pH����7���������ԣ�������̪��Һ����ÿ�Ȫˮ��Ʒ�У����Ժ�ɫ������Ȼ��Ȫˮ�к��ж������ʣ�������һ������̼�����ƿ���������θ�����֢���䷴Ӧԭ���ǣ�NaHCO3+HCl=NaCl+H2O+CO2������3���������ʵ����ʺ���;��ϸ�����Ԫ�ؿ�֪���ٿ������Ϸ��ϵ���������أ���ѧʽ�ǣ�KNO3������ˮ����ʹ��ɫʯ����Һ����������̼�ᣮ��ѧʽ�ǣ�H2CO3���ۿ����������ϵļ����������ƣ���ѧʽ�ǣ�Ca��OH��2����������ʻԱ����ǰ��ֹ���õ������Ǿƾ�����ѧʽ�ǣ�C2H5OH��
�ʴ�Ϊ����1��Ԫ�أ� ![]() ��13��16����2��SO42�����죬NaHCO3+HCl=NaCl+H2O+CO2������3����KNO3����H2CO3����Ca��OH��2����C2H5OH��
��13��16����2��SO42�����죬NaHCO3+HCl=NaCl+H2O+CO2������3����KNO3����H2CO3����Ca��OH��2����C2H5OH��

����Ŀ�����г�ȥ���ʵķ����У���ȷ���ǣ�������
�� �� | �� �� | �����ʵķ��� | |
A | CuO | Cu | ���������ϡ���ᣬ���� |
B | FeCl3��Һ | CuCl2��Һ | ������������ۣ����� |
C | CO | CO2 | ͨ�����ȵ�����ͭ |
D | KOH��Һ | K2CO3��Һ | ��������������������Һ������ |
A.AB.BC.CD.D
����Ŀ������С�鰴��ͼ��ʾʵ��̽�������ȼ�ղ������˲�ͬ��ʵ������
���飺�ձ��ڱ�����ɫҺ��
���飺�ձ��ڱ�����ɫҺ�Σ��ձ��ײ������к�ɫ����
��������⡿ ͬѧ�Dz��Ľ̲�ʵ�飬��֪��ɫҺ����ˮ������ɫ������ʲô�أ�
�����롿 ͬѧ�Dz����ɫ�������Ҫ�ɷ���̼��
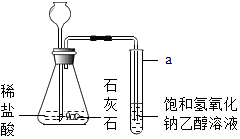
��1����ʵ����֤��������ͼ��ʾװ�ã��ס���С���ͬѧ�ֱ���������·���������֤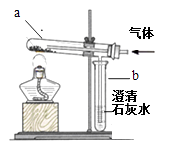
ʵ����� | ʵ������ | |
���� | ȡ�����ú�ɫ������a�У�ͨ���������ȼ�ƾ��Ƽ��ȡ� | ��ɫ����ȼ�գ��� �� b����Һ����ǡ� |
���� | ȡ�����ú�ɫ������a�У�ͨ�� �� �� ��ȼ�ƾ��Ƽ��ȡ� | ��ɫ�������ȼ�գ������⣬b����Һ����ǡ� |
��2������������ۡ�
ʵ�����ʱ��ֹͣͨ�����壬����ʵ�����˳��Ӧ��(����ĸ���)��
A.Ϩ��ƾ��ƣ�ֹͣ����
B.���Թ�b����
��3��b�е�ʵ������˵����ɫ����ȼ�������� �� �ɴ˿��ƶϲ�����ȷ����������
��4������˼��
��һ��ʵ�鷢�֣����ڻ����Ϸ����ձ�λ��Խ�ͣ�������ɫ����Խ�ࡣ�������Ͽ�֪������+����(����)��������̼ + ˮ������+����(����)�� һ����̼ + ˮ��
�ɴ��Ʋ�����ʵ�������ɫ�����ԭ������