题目内容
某化学兴趣小组在老师指导下制取、干燥、收集氨气,并探究氨气的一些性质。
资料卡片:氨气通常情况下是有刺激性气味的无色气体,密度比空气小,极易溶于水,易液化,液氨可作制冷剂。
加热熟石灰和氯化铵固体混合物的方法可以生成氨气。如要快速产生氨气,可以将浓氨水滴加到生石灰中得到。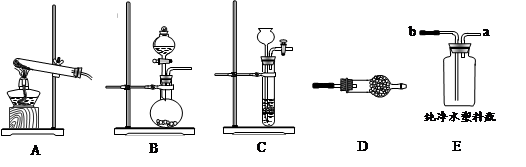
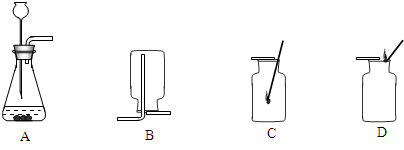
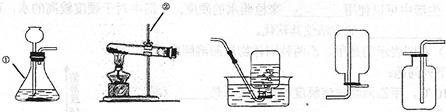
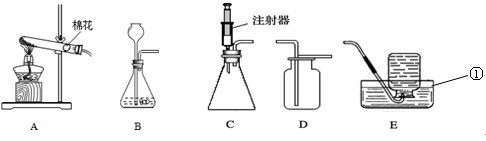
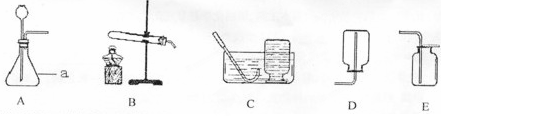
(1)利用A装置制取氨气的化学方程式为 。将浓氨水滴加到生石灰快速产生氨气,发生装置最好选用 (选填装置编号)。请写出生石灰在此反应中的两个作用: , 。
(2)干燥氨气可以将气体通过装有 (填化学式)的装置D。
(3)兴趣小组计划用E装置收氨气,简述判断氨气已经集满的方法。 。
(4)按图连接仪器后,计划在纯净水塑料瓶内引发喷泉,你会采取怎样的操作? 。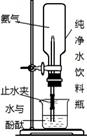
⑸ 试验后为处理纯净水塑料瓶内存在的氨水(NH3?H2O)可以加入少量稀硫酸,发生反应的化学方程式为 。
(1)Ca(OH)2+(NH4)2SO4△CaSO4+2H2O+2NH3↑(2分) B(1分) CaO与水反应,减少了溶剂(1分)CaO遇水放热,降低了NH3的溶解度(1分)(答案合理给分)
(2)CaO或NaOH(1分)
(3)将湿润的红色石蕊试纸放在b端,若试纸变蓝色,说明氨气已经集满。(2分)
(注意:答对“b”端观察现象1分,答对合适的试剂如“湿润的pH试纸、滴有酚酞的棉球”和现象1分)
(4)挤压塑料瓶,使氨气排入水中(1分)(答案合理给分)
(5)2NH3?H2O+H2SO4 =(NH4)2SO4+2H2O(2分)
解析试题分析:(1)氢氧化钙和氯化铵反应生成氯化钙、水和氨气;将浓氨水滴加到生石灰中会快速产生氨气,应该用容积较大的容器;生石灰在此反应中的两个作用:CaO与水反应,减少了溶剂;CaO遇水放热,降低了NH3的溶解度;
(2)氧化钙、氢氧化钠具有吸水性,可以用作氨气的干燥剂;
(3)氨水显碱性,能使红色石蕊试纸变蓝色:判断氨气已经集满的方法是:将湿润的红色石蕊试纸放在b端,若试纸变蓝色,说明氨气已经集满;
(4)氨气极易溶于水,溶于水后使纯净水塑料瓶内的压强减小,形成喷泉;所以应打开止水夹,挤压塑料瓶,使氨气排入水中;
(5)氨水和硫酸反应生成硫酸铵和水,准确写出化学方程式即可.
考点:常用气体的发生装置和收集装置与选取方法;气体的干燥(除水);生石灰的性质与用途;书写化学方程式、文字表达式、电离方程式

 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案常温常压下在实验室收集NH3(气体),与选择收集方法无关的信息是( )
| A.NH3的密度 | B.NH3在水中的溶解性 | C.空气的密度 | D.NH3的质量 |
如图所示装置气密性良好、要使注射器中的活塞向右移动,使用的液体M和固体N可能是( )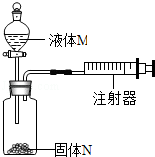
①稀盐酸和石灰石;②稀硫酸和锌;③水和氢氧化钠;④水和硝酸铵.
| A.①②③④ | B.①②③ | C.①②④ | D.②③④ |