题目内容
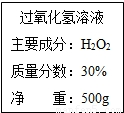
(2007?太原)过氧化氢溶液在存放过程中会缓慢分解.右图为实验室保存的一瓶过氧化氢溶液的标签.某小组同学为了解过氧化氢的分解情况,取5g该溶液共制得0.64g氧气.试分析计算(1)求5g该溶液的溶质的质量分数.
(2)这瓶过氧化氢溶液在保存过程中已经分解的过氧化氢的质量.
【答案】分析:(1)根据过氧化氢缓慢分解的化学方程式和生成氧气的质量,即可计算出5g该溶液的溶质的质量,然后根据溶质质量分数= ×100%计算即可;
×100%计算即可;
(2)根据标签所示计算出这瓶过氧化氢溶液原有过氧化氢的质量,然后根据过氧化氢缓慢分解的化学方程式,得出分解掉的过氧化氢的质量与生成水的关系式,再根据质量分数公式进行计算,即可得出分解掉的过氧化氢的质量.
解答:解:(1)设5g该溶液的溶质的质量为x,
2H2O2═2H2O+O2↑
68 32
x 0.64g
∴
解之得:x=1.36g,
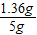 ×100%=27.2%.
×100%=27.2%.
(2)这瓶过氧化氢溶液原有过氧化氢的质量为:500g×30%=150g,
设分解掉的过氧化氢的质量为X,同时生成的水质量为Y,
2H2O2═2H2O+O2↑
68 36
X Y
∴68:36=x:y,
∴y=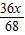 ,
,
∴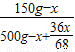 =27.2%,
=27.2%,
解之得;x=16.09g,
答:(1)5g该溶液的溶质的质量分数为27.2%;
(2)这瓶过氧化氢溶液在保存过程中已经分解的过氧化氢的质量为16.09g.
点评:本题主要考查学生运用化学方程式和质量分数公式进行计算的能力.
 ×100%计算即可;
×100%计算即可;(2)根据标签所示计算出这瓶过氧化氢溶液原有过氧化氢的质量,然后根据过氧化氢缓慢分解的化学方程式,得出分解掉的过氧化氢的质量与生成水的关系式,再根据质量分数公式进行计算,即可得出分解掉的过氧化氢的质量.
解答:解:(1)设5g该溶液的溶质的质量为x,
2H2O2═2H2O+O2↑
68 32
x 0.64g
∴

解之得:x=1.36g,
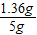 ×100%=27.2%.
×100%=27.2%.(2)这瓶过氧化氢溶液原有过氧化氢的质量为:500g×30%=150g,
设分解掉的过氧化氢的质量为X,同时生成的水质量为Y,
2H2O2═2H2O+O2↑
68 36
X Y
∴68:36=x:y,
∴y=
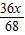 ,
,∴
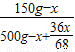 =27.2%,
=27.2%,解之得;x=16.09g,
答:(1)5g该溶液的溶质的质量分数为27.2%;
(2)这瓶过氧化氢溶液在保存过程中已经分解的过氧化氢的质量为16.09g.
点评:本题主要考查学生运用化学方程式和质量分数公式进行计算的能力.

练习册系列答案
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目