��Ŀ����
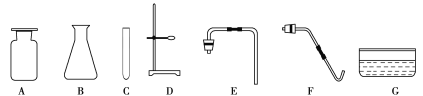
����Ŀ��ij��ѧ�о���ѧϰС����ѧϰ��Ļ�ѧ����ʱ�������ʵ�鷽������������ͼ��ʾ��ʵ�飬���������ϵ�֪��Na2CO3��Һ�ͳ����ʯ��ˮ���ʼ���(pH��7)��CaCl2��Һ������(pH=7)��
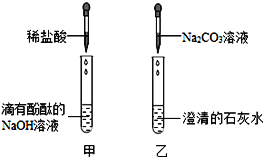
(1)��ʵ���У����з�̪������������Һ��___ɫ����μ���ϡ���ᣬֱ����Һǡ�ó���ɫΪֹ��
(2)��ʵ���Թ��ڲ�����ɫ�������䷢����Ӧ�Ļ�ѧ����ʽΪ___
(3)ʵ�������ͬѧ�ǽ��ס�������ʵ��ķ�Һ����ͬһ���ձ��У��۲쵽��Һ�ʻ��Dz��Ժ�ɫ���ɴ˷�����֪��
�ٷ�Һ�г�̼��ơ��Ȼ��ơ�ˮ��ָʾ���⣬һ��������____��
����������ʵ����̣�����Ϊ�����Һ�ʼ��Ե�������ɹ���___�ֿ���.
���𰸡��� Ca(OH)2��Na2CO3=CaCO3����2NaOH NaOH 3
��������
ϡ������������Ʒ�Ӧ�����Ȼ��ƺ�ˮ��̼���ƺ��������Ʒ�Ӧ����̼��ƺ��������ơ�
(1)��ʵ���У�����ʹ��̪��Һ�Ժ�ɫ���ʵ��з�̪������������Һ�ʺ�ɫ����μ���ϡ���ᣬϡ������������Ʒ�Ӧ�����Ȼ��ƺ�ˮ��ֱ����Һǡ�ó���ɫΪֹ��
(2)��ʵ���Թ��ڲ�����ɫ�������䷢���ķ�Ӧ��̼���ƺ��������Ʒ�Ӧ����̼��ƺ��������ƣ���Ӧ�Ļ�ѧ����ʽΪ![]() ��
��
(3) �ٷ�Һ�ʻ��Dz��Ժ�ɫ����Һ�г�̼��ơ��Ȼ��ơ�ˮ��ָʾ���⣬һ��������![]() ��
��
����������ʵ����̣�����Ϊ�����Һ�ʼ��Ե�������ɿ������������ƻ�̼���ƻ��������ƺ�̼���ƣ�����3�ֿ��ܡ�

����Ŀ��MgSO4��Na2SO4���ܽ�ȱ����ܽ���������¡�����˵����ȷ���ǣ� ��
�¶�/�� | 20 | 30 | 40 | 50 | 60 | 70 | |
�ܽ�� S/g | MgSO4 | 33.7 | 38.9 | 44.5 | 50.6 | 54.6 | 55.8 |
Na2SO4 | 19.5 | 40.8 | 48.8 | 47.5 | 45.3 | 44.8 | |

A. ��ΪNa2SO4
B. t3��Ӧ����40����50��֮��
C. t4���ҵı�����Һ�����µ�t1���Ĺ����У�һֱ�о�������
D. b��c���ҵı�����Һ��������������ȣ��Ҵ���a��ı�����Һ������������
����Ŀ���ᡢ����Ǿ��꼶��ѧѧϰ����Ҫ֪ʶ���������Ǿ��й㷺����;��
��1�����й����ᡢ��ε�˵����ȷ����________________��
A ����������ܷ�Ӧ�����κ����� B �ܹ������κ�ˮ�ķ�Ӧ�������кͷ�Ӧ
C ��ͼ������Ԫ�� D �ᡢ���֮�䶼�ܷ������ֽⷴӦ
��2����ͼ�֮���ܹ������кͷ�Ӧ����������з�̪������������Һ����μ���ϡ���ᣬ�÷�Ӧ�Ļ�ѧ����ʽΪ________________�����μ�һ����ϡ�������Һ��Ϊ��ɫ����÷�Ӧ����Һ�� pH��6������Һ�д��ڵ�������Ϊ________________ (�����ӷ���)��
��3��ij��ɫ�����п��ܺ���̼���ơ����ᱵ���������ơ�����ͭ�е�һ�ֻ��֣�Ϊȷ���ù� ��ɷ֣��ֽ�������ʵ�飺
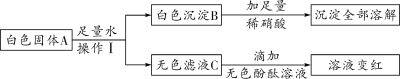
�ٸ�������ʵ�������A ��һ�����е�������________________��C ��һ�����е�������
________________��
��Ϊ��һ��ȷ������ A �п��ܴ��ڵ����ʣ�����Һ C ����ʵ�飬����±���
ʵ����� | ���� | ���� |
________________ | ________________ | A������������ |
��4���� 50 g ϡ������� 50 g ����������Һ��ǡ����ȫ��Ӧ��������Һ�����ʵ��������� Ϊ 5.85%���Լ�������������Һ�����ʵ�����������________________
����Ŀ�������±�����ʵ�飬�й�˵���������������
������KOH��Һ�еμ�CuSO4��Һ | ������BaCl2��Һ�еμ�CuSO4��Һ | |
���� | �� | ��ɫ���� |
��ѧ����ʽ | 2KOH + CuSO4 =Cu(OH)2��+ K2SO4 | �� |
A. ������ɫ����
B. �ڷ�Ӧ�Ļ�ѧ����ʽΪCuSO4 +BaCl2 =BaSO4��+CuCl2
C. ������Ӧ�����ڸ��ֽⷴӦ
D. ֻҪ�г������ɵķ�Ӧ�����ڸ��ֽⷴӦ