题目内容
(6分)为了验证二氧化碳与氢氧化钠可以发生化学反应,某小组用下图所示装置进行实验。请回答下列问题: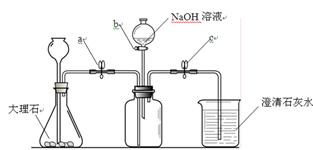
(1)打开止水夹a和c,从长颈漏斗向锥形瓶中注入稀盐酸至 时停止。
(2)当观察到烧杯中有大量白色沉淀产生时,说明集气瓶中已集满二氧化碳气体。然后进行的操作是 ,关闭活塞b,轻轻振荡集气瓶。一段时间后可观察到 ,证明二氧化碳与氢氧化钠发生了化学反应,该反应的化学方程式为 。
(3)小红认为仅做上述实验有不足之处,应利用上图装置做一个对比实验。该对比实验只需将所用的氢氧化钠溶液换成 即可。
(4)为了保证实验的成功,应在实验前对装置的气密性进行检验(不另加仪器),方法为 。
(1)长颈漏斗下端管口浸没在液面下(液封)
(2)关闭止水夹a,打开活塞b(止水夹、活塞不写给分),向集气瓶中加入适量的NaOH溶液 烧杯中的混浊液体从导管倒吸入集气瓶中 CO2 + 2NaOH ="=" Na2CO3 + H2O (3)水
(4)打开止水夹a(关闭活塞b和止水夹c),从长颈漏斗向锥形瓶中注入水至长颈漏斗下端管口浸没在液面下,继续加水,此时长颈漏斗中有一段水柱高于锥形瓶内液面,放置一段时间,液面不变化。说明气密性良好。(建议同时答出取样、操作、现象和结论;结论必须为气密性良好)
解析试题分析:(1)固体和液体反应制气体时,长颈漏斗的下端要插入液面以下,防止气体从漏斗逸出。
(2)关闭止水夹a,打开活塞b,向集气瓶中加入适量的NaOH溶液,由于二氧化碳和NaOH反应生成碳酸钠和水,即CO2+2NaOH=Na2CO3+H2O,故造成集气瓶内部气体的量减少,则集气瓶内部压强减小,在大气压的作用下烧杯中的石灰水就会进入集气瓶。
(3)由于二氧化碳不仅可溶于水,而且还能和水反应,氢氧化钠溶液中又存在有大量的溶剂——水,故仅做该实验不足以证明二氧化碳与氢氧化钠发生了化学反应,因此还需要一个对比实验;根据控制变量法的原则,除变量外其他条件要相同,故该对比实验只需将所用的氢氧化钠溶液换成水即可。
(4)气密性检查,是利用了密闭空间内压强能够改变来实现的,故如果气密性良好,打开止水夹a(关闭活塞b和止水夹c),从长颈漏斗向锥形瓶中注入水至长颈漏斗下端管口浸没在液面下,随着气体的体积减小,内部压强增大,内部压强和大气压就会出现一个差值,即在长颈漏斗中出现一个高于锥形瓶液面的水柱,说明气密性良好。
考点:探究二氧化碳的性质,检查装置的气密性
点评:对于验证型实验探究,要熟记物质的性质或变化规律,根据给出的实验设计方案,进行实验、分析和探究,并通过观察、记录和分析的实验现象,来验证该物质的性质或变化规律等。

 智慧小复习系列答案
智慧小复习系列答案
 (2008?河北)人的胃液里含有适量的盐酸,可以帮助消化,但如果胃酸分泌过多,人会感到胃痛.小军拿来了一种抗酸药(治疗胃酸过多的药物),该药物说明书的部分内容如图所示.
(2008?河北)人的胃液里含有适量的盐酸,可以帮助消化,但如果胃酸分泌过多,人会感到胃痛.小军拿来了一种抗酸药(治疗胃酸过多的药物),该药物说明书的部分内容如图所示.