题目内容
学完“二氧化碳性质的探究”后,小明同学觉得按照实验
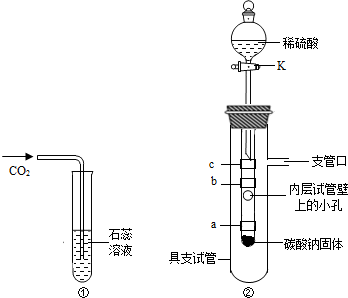
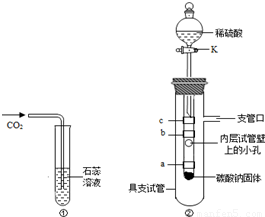
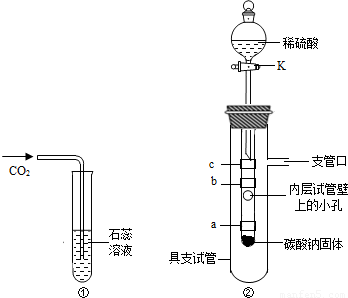
(图①)不能完全说明是什么物质使紫色石蕊溶液变红色,他和小娜同学进行了如下实验探究:
【猜想与假设】
猜想一:水使紫色石蕊溶液变红
猜想二:二氧化碳使紫色石蕊溶液变红猜想三:二氧化碳与水反应生成的新物质使紫色石蕊溶液变红
【查阅资料与实验准备】
将纸条浸泡在紫色石蕊溶液中,晾干后可制得紫色石蕊试纸.
自制的紫色石蕊试纸遇酸变红色,遇碱溶液变蓝色.
【设计与实验】
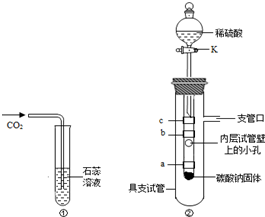
小明同学设立了实验装置如图②.
图中a、b、c为紫色石蕊试纸,缠绕在小试管上,其中a和c用水湿润.
(1)a、c石蕊试纸用水润湿后仍为紫色,说明猜想
(2)打开活塞K,滴入稀硫酸,发生反应的方程式为
观察并解释实验现象:
①试纸b没有明显变化,得出结论:猜想
②试纸a、c由紫色变为红色,得出结论:猜想
③试纸
【交流与反思】
(3)小娜同学认为,上图装置还可以同时验证:A.二氧化碳能使澄清石灰水变浑浊;B.二氧化碳不能燃烧不支持燃烧.
为了分别完成小娜同学的两个验证实验,请对上面的实验进行简单的改进:
A.
(4)该实验不用盐酸而用硫酸是为了防止HCl气体对试纸变色的干扰;试分析此实验用碳酸钠而不用大理石的原因
(图①)不能完全说明是什么物质使紫色石蕊溶液变红色,他和小娜同学进行了如下实验探究:

【猜想与假设】
猜想一:水使紫色石蕊溶液变红
猜想二:二氧化碳使紫色石蕊溶液变红猜想三:二氧化碳与水反应生成的新物质使紫色石蕊溶液变红
【查阅资料与实验准备】
将纸条浸泡在紫色石蕊溶液中,晾干后可制得紫色石蕊试纸.
自制的紫色石蕊试纸遇酸变红色,遇碱溶液变蓝色.
【设计与实验】
小明同学设立了实验装置如图②.
图中a、b、c为紫色石蕊试纸,缠绕在小试管上,其中a和c用水湿润.
(1)a、c石蕊试纸用水润湿后仍为紫色,说明猜想
一
一
不正确.(2)打开活塞K,滴入稀硫酸,发生反应的方程式为
Na2CO3+H2SO4═Na2SO4+H2O+CO2
Na2CO3+H2SO4═Na2SO4+H2O+CO2
.观察并解释实验现象:
①试纸b没有明显变化,得出结论:猜想
二
二
不正确.②试纸a、c由紫色变为红色,得出结论:猜想
三
三
正确.相关化学方程式为H2O+CO2═H2CO3
H2O+CO2═H2CO3
.③试纸
a
a
首先变色,其原因是CO2密度大于空气
CO2密度大于空气
.【交流与反思】
(3)小娜同学认为,上图装置还可以同时验证:A.二氧化碳能使澄清石灰水变浑浊;B.二氧化碳不能燃烧不支持燃烧.
为了分别完成小娜同学的两个验证实验,请对上面的实验进行简单的改进:
A.
具支试管中倒入少量澄清石灰水
具支试管中倒入少量澄清石灰水
;B.支管口放一燃着的木条进行验证二氧化碳是否具有可燃性
支管口放一燃着的木条进行验证二氧化碳是否具有可燃性
.(4)该实验不用盐酸而用硫酸是为了防止HCl气体对试纸变色的干扰;试分析此实验用碳酸钠而不用大理石的原因
碳酸钙会与硫酸生成微溶的硫酸钙覆盖在表面阻碍反应进行
碳酸钙会与硫酸生成微溶的硫酸钙覆盖在表面阻碍反应进行
(写一点).分析:【设计与实验】(1)紫色石蕊试纸被水润湿后不变色,说明水不能使紫色石蕊试液变色,可以据此解答该题;
(2)碳酸钠和稀硫酸反应生成了硫酸钠、水和二氧化碳,可以据此写出该反应的化学方程式;
①试纸B为干燥的试纸,而b没有变色,说明干燥的二氧化碳不能使石蕊试液变色,可以据此解答该题;
②a、c为用水湿润的试纸,变色则说明二氧化碳和水反应生成碳酸,可以据此写出该反应的化学方程式;
③二氧化碳的密度比空气大,所以可以知道应该是试纸a先变色,可以据此解答;
【交流与反思】(3)检验二氧化碳可以将澄清石灰水倒入具支试管中,而检验二氧化碳是否支持燃烧可以将燃着的木条放在支管口,可以据此解答该题;
(4)碳酸钙会与硫酸生成微溶的硫酸钙覆盖在表面阻碍反应进行,可以据此解答该题.
(2)碳酸钠和稀硫酸反应生成了硫酸钠、水和二氧化碳,可以据此写出该反应的化学方程式;
①试纸B为干燥的试纸,而b没有变色,说明干燥的二氧化碳不能使石蕊试液变色,可以据此解答该题;
②a、c为用水湿润的试纸,变色则说明二氧化碳和水反应生成碳酸,可以据此写出该反应的化学方程式;
③二氧化碳的密度比空气大,所以可以知道应该是试纸a先变色,可以据此解答;
【交流与反思】(3)检验二氧化碳可以将澄清石灰水倒入具支试管中,而检验二氧化碳是否支持燃烧可以将燃着的木条放在支管口,可以据此解答该题;
(4)碳酸钙会与硫酸生成微溶的硫酸钙覆盖在表面阻碍反应进行,可以据此解答该题.
解答:解:【设计与实验】(1)紫色石蕊试纸被水润湿后不变色,说明水不能使紫色石蕊试液变色,即猜想一是错误的;
(2)碳酸钠和稀硫酸反应生成了硫酸钠、水和二氧化碳,该反应的化学方程式为:Na2CO3+H2SO4═Na2SO4+H2O+CO2;
①试纸B为干燥的试纸,而b没有变色,说明干燥的二氧化碳不能使石蕊试液变色,说明猜想二是错误的;
②a、c为用水湿润的试纸,变色则说明二氧化碳和水反应生成碳酸,即猜想三是正确的,该反应的化学方程式为:H2O+CO2═H2CO3;
③二氧化碳的密度比空气大,所以可以知道应该是试纸a先变色;
【交流与反思】(3)检验二氧化碳可以使澄清石灰水变浑浊,可以将澄清石灰水倒入具支试管中,而检验二氧化碳是否支持燃烧以及是否燃烧可以将燃着的木条放在支管口即可;
(4)碳酸钙会与硫酸生成微溶的硫酸钙覆盖在表面阻碍反应进行,所以不能用大理石来代替碳酸钠.
故答案为:(1)一;
(2)Na2CO3+H2SO4═Na2SO4+H2O+CO2;
①二;
②三;H2O+CO2═H2CO3;
③a;CO2密度大于空气;
(3)A.具支试管中倒入少量澄清石灰水;B.支管口放一燃着的木条进行验证二氧化碳是否具有可燃性;
(4)碳酸钙会与硫酸生成微溶的硫酸钙覆盖在表面阻碍反应进行.
(2)碳酸钠和稀硫酸反应生成了硫酸钠、水和二氧化碳,该反应的化学方程式为:Na2CO3+H2SO4═Na2SO4+H2O+CO2;
①试纸B为干燥的试纸,而b没有变色,说明干燥的二氧化碳不能使石蕊试液变色,说明猜想二是错误的;
②a、c为用水湿润的试纸,变色则说明二氧化碳和水反应生成碳酸,即猜想三是正确的,该反应的化学方程式为:H2O+CO2═H2CO3;
③二氧化碳的密度比空气大,所以可以知道应该是试纸a先变色;
【交流与反思】(3)检验二氧化碳可以使澄清石灰水变浑浊,可以将澄清石灰水倒入具支试管中,而检验二氧化碳是否支持燃烧以及是否燃烧可以将燃着的木条放在支管口即可;
(4)碳酸钙会与硫酸生成微溶的硫酸钙覆盖在表面阻碍反应进行,所以不能用大理石来代替碳酸钠.
故答案为:(1)一;
(2)Na2CO3+H2SO4═Na2SO4+H2O+CO2;
①二;
②三;H2O+CO2═H2CO3;
③a;CO2密度大于空气;
(3)A.具支试管中倒入少量澄清石灰水;B.支管口放一燃着的木条进行验证二氧化碳是否具有可燃性;
(4)碳酸钙会与硫酸生成微溶的硫酸钙覆盖在表面阻碍反应进行.
点评:解答本题关键是要根据资料中:紫色石蕊试纸遇酸变红色,再结合二氧化碳与水反应生成碳酸,来进一步分析本题,根据装置的特点来改进验证二氧化碳的性质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目