题目内容
某二氧化锰样品中含有杂质炭,为测定该样品中二氧化锰的质量分数,某兴趣小组设计了如下实验方案:在一定量的样品中通入干燥纯净的氧气,使杂质炭在加热条件下反应生成CO2来进行分析测定.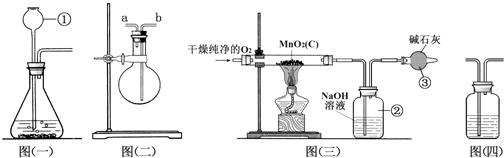
(1)仪器①的名称是
(2)用图(二)装置可收集和干燥氧气:若烧瓶充满水来收集氧气,气体应从
(3)图(三)是用干燥纯净的O2与样品反应来测定二氧化锰质量分数的装置,装置③中装有碱石灰,其作用是
(4)为验证图(三)中装置②已将CO2吸收完全,可在装置②与③之间加入图(四)装置进行证明,则图(四)装置中加入的试剂为
A.NaOH溶液 B.澄清石灰水 C.浓硫酸
(5)称取5.0g二氧化锰样品进行实验,图㈢中装置②反应前后的质量差为1.1g,则样品中二氧化锰的质量分数为
分析:本题考查了实验室制取气体原理、收集气体的方法、正确干燥气体的操作、定量排水收集气体的方法.
解答:解:(1)仪器①长颈漏斗,图㈠装置可用于反应物是,固体和液体反应,反应在常温下进行的反应.
(2)用图(二)装置干燥气体时要长导管进气,短导管出气;收集气体时,注意短导管进气,长导管出水.
(3)图(三)中碱石灰的作用是吸收空气中的二氧化碳和水蒸气,以防止空气中的氢氧化钠和碱石灰进入到空气中使试验测量结果不准.
(4)验证二氧化碳气体可用澄清的石灰水.
(5)解:根据题意反应后生成二氧化碳的质量为1.1g,设生成1.1gCO2需碳的质量为x
C+O2
CO2
12 44
x 1.1g
=
x=0.3g
则样品中二氧化锰的质量分数为:
×100%=94%
故答案为:(1)长颈漏斗,2H2O2
2H2O+O2 ↑,Zn+H2SO4 ═ZnSO4+H2↑,CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)a,b
(3)防止空气中的二氧化碳和水分时入氢氧化钠溶液
(4)B.
(5)94%.
(2)用图(二)装置干燥气体时要长导管进气,短导管出气;收集气体时,注意短导管进气,长导管出水.
(3)图(三)中碱石灰的作用是吸收空气中的二氧化碳和水蒸气,以防止空气中的氢氧化钠和碱石灰进入到空气中使试验测量结果不准.
(4)验证二氧化碳气体可用澄清的石灰水.
(5)解:根据题意反应后生成二氧化碳的质量为1.1g,设生成1.1gCO2需碳的质量为x
C+O2
| ||
12 44
x 1.1g
| 12 |
| 44 |
| x |
| 1.1g |
x=0.3g
则样品中二氧化锰的质量分数为:
| 5g-0.3g |
| 5g |
故答案为:(1)长颈漏斗,2H2O2
| ||
(2)a,b
(3)防止空气中的二氧化碳和水分时入氢氧化钠溶液
(4)B.
(5)94%.
点评:要想解答好这类题目,要熟记常见气体的检验与除杂方法及理论依据,还有氧气、氢气、二氧化碳等气体的相关知识,有时还需弄清图示信息,以及有关的注意事项等等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目