题目内容
【题目】现有下列九种物质:红磷、铁丝、木炭、氧气、水、氧化铜、稀盐酸、高锰酸钾、石灰石。从中选择适当的物质按下列要求写出有关反应的化学方程式:
(1)生成白色固体的化合反应:_______________________________________。
(2)生成两种气体的分解反应:_______________________________________。
(3)一种单质和一种化合物的反应:___________________________________。
(4)常温下两种物质的反应:_________________________________________。
【答案】4P+5O2![]() 2P2O5 2H2O
2P2O5 2H2O![]() 2H2↑+O2↑ C+2CuO
2H2↑+O2↑ C+2CuO![]() 2Cu + CO2↑ CaCO3+2HCl==CaCl2+H2O+CO2↑或CuO+2HCI==CuCl2+H2O
2Cu + CO2↑ CaCO3+2HCl==CaCl2+H2O+CO2↑或CuO+2HCI==CuCl2+H2O
【解析】
(1)红磷燃烧生成白色固体五氧化二磷,反应的化学方程式为:4P+5O2![]() 2P2O5,由多种物质反应生成一种物质,符合化合反应定义 。
2P2O5,由多种物质反应生成一种物质,符合化合反应定义 。
(2)电解水生成氢气和氧气,反应的化学方程式为2H2O![]() 2H2↑+O2↑,由一种物质分解成多种物质,符合分解反应定义。
2H2↑+O2↑,由一种物质分解成多种物质,符合分解反应定义。
(3)高温条件下,化合物氧化铜和碳单质能发生反应生成铜和二氧化碳,反应的化学方程式为C+2CuO![]() 2Cu + CO2↑。
2Cu + CO2↑。
(4)通常情况下,稀盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,和氧化铜反应生成氯
化铜和水,反应的化学方程式为CaCO3+2HCl==CaCl2+H2O+CO2↑或CuO+2HCI==CuCl2+H2O。

【题目】“配制一定溶质质量分数的氯化钠溶液”是初中化学的基础实验之一。请回答下列问题:
(1)现欲配制一瓶500g溶质质量分数为0.9%的氯化钠溶液,需氯化钠固体______g.
(2)下列实验操作与分析均正确的一组是__________(填序号)。
项目 | 实验操作 | 分析 |
A | 称量时,将取出的过量氯化钠放回原瓶 | 节约药品 |
B | 溶解氯化钠时用玻璃棒搅拌 | 增大氯化钠的溶解度 |
C | 称取氯化钠时,在天平两边托盘上各放一张质量相等的纸 | 整洁美观 |
D | 量取所需水时,视线与量筒内液体凹液面的最低处保持水 | 准确读数 |
(3)实验室若用溶质质量分数为15%的氯化钠溶液配制成溶质质量分数为5%的氯化钠溶液60g,此时需要用到的玻璃仪器有烧杯、玻璃棒、量筒和________,需要加水的质量为____g.
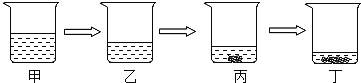
(4)实验室若用恒温蒸发的方法将15%的氯化钠溶液变成饱和溶液,其过程如下图所示,与丙烧杯中溶液溶质质量分数一定相同的是_________(填序号)烧杯中的溶液。