题目内容
【题目】氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:
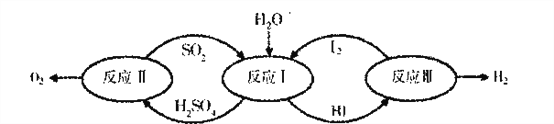
(l)反应I中,发生反应的化学方程式为_________________。
(2)反应Ⅲ中,反应前后化合价发生改变的元素是_______,发生反应的基本类型为_______反应。
(3)在整个反应过程中,可循环使用的物质有_________(写出一种即可),利用热化学硫碘循环分解水制氢的优点________________。
【答案】 2H2O + I2 + SO2 = 2HI + H2SO4 H和I 分解 SO2、H2SO4、I2、HI 节约能源,降低生产成本
【解析】(1)反应I中是二氧化硫和碘和水反应生成碘化氢和硫酸,反应方程式为2H2O + I2 + SO2 = 2HI + H2SO4;
(2)反应Ⅲ中,有单质碘和氢气生成,故有化合价变化的元素是碘和氢;该反应是碘化氢反应生成碘和氢气,是分解反应;
(3)在整个反应过程中,可循环使用的物质有SO2、H2SO4、I2、HI;该方法制取氢气的优点是约能源,降低生产成本

【题目】化学兴趣小组对“锌与稀硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与稀硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】①可能与稀硫酸的溶质质量分数有关;②可能与锌的形状有关。
【设计并实验】兴趣小组用100mL不同质量分数的稀硫酸和5g不同形状的锌进行如下实验(时间为3分钟)。

(1)锌与硫酸反应的化学方程式为_______________________________。
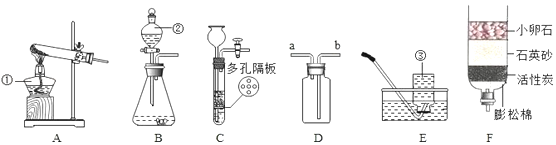
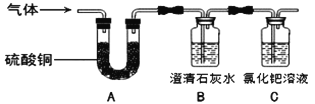
(2)如图所示装置收集并测量氢气的体积,则正确的链接顺序是:
氢气→______________________(填导管口序号)。
【收集证据】
(3)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是______。
【得出结论】依据上表得出的结论是____________________________________。
【反思评价】
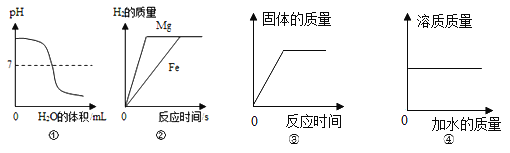
(4)下表是兴趣小组第①组实验根据前6分钟记录详细数据(每分钟记录一次产生氢气的体积)。
时段 (均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
H2的体积/mL | 3.1 | 16.7 | 11.9 | 9.6 | 7.6 | 6.0 |
请解释锌与稀硫酸反应由快变慢的原因____________________________________。
(5)锌与硫酸反应的快慢可能还会受_____________因素影响,如果用实验验证该因素对反应快慢的影响,应该控制________________因素不同,而其他因素则相同。
【题目】同学们通过以下实验,探究某些酸、碱、盐之间能否发生复分解反应。
(查阅资料)BaSO4是白色固体,难溶于水,也不与盐酸反应。
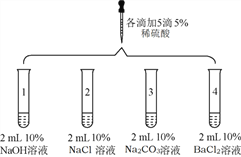
(实验一)同学们取4支试管,分别加入一定量4种溶液于试管中,再分别滴加少量的稀硫酸。
实验装置 | 实验现象 |
| 1号试管中无明显现象 |
2号试管中无明显现象 | |
3号试管中_____ | |
4号试管中有白色沉淀产生 |
(1)3号试管中的实验现象是_____。
(2)4号试管中发生复分解反应的化学方程式为_____。
(提出问题)3号、4号试管中的现象能证明硫酸与Na2CO3、BaCl2发生了复分解反应。1号、2号试管中均没有观察到明显现象,如何证明硫酸与NaOH、NaCl是否发生了复分解反应?
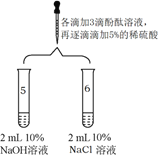
(实验二)同学们又进行了以下实验。
实验装置 | 实验现象 |
| 5号试管中,滴加酚酞溶液后,溶液由无色变为红色;滴加一定量稀硫酸后,溶液由红色变为无色 |
6号试管中始终无明显现象 |
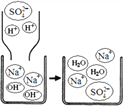
(3)5号试管中的现象能证明NaOH与稀硫酸发生了复分解反应。下图为反应的微观示意图,从微观粒子变化的角度分析,该反应的实质是_____。
(反思与评价)
(4)同学们发现3号、4号试管中的微粒数也有变化:4号试管中的Ba2+、SO42-因生成沉淀而减少,3号试管中减少的微粒是_____。
(5)欲进一步探究2号试管中的两种物质是否发生了复分解反应,又补充了以下实验。
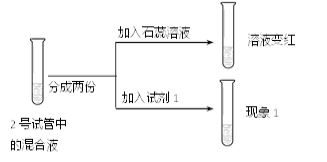
该实验证明两种物质不能发生复分解反应。请结合实验中的信息,回答下列问题:
①滴加石蕊溶液的目的是_____。
②试剂1和现象1分别是_____。
(6)根据此次探究活动,你认为下列说法正确的是_____(填序号)。
A.酸、碱、盐之间并不是都能发生复分解反应
B.从微观上看,复分解反应的实质是溶液中某些离子相互结合使离子数目减少
C.判断化学反应发生,可依据有新物质生成,也可依据某一反应物消失
D.证明复分解反应没有发生,可验证某一反应物依然存在