题目内容
下列说法正确的是
- A.镁条的质量等于它燃烧后生成物的质量
- B.蜡烛燃烧时逐渐变短,不符合质量守恒定律
- C.高锰酸钾受热分解的总质量等于生成物的总质量
- D.12g碳和16g氧气反应,可生成28g二氧化碳
C
分析:根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变.
解答:A、镁条燃烧,是镁与氧气反应的过程,故它燃烧后生成物的质量比镁条的质量多出了参与反应的氧气的质量,故A不适合;
B、蜡烛燃烧时逐渐变短,是因为生成了二氧化碳和水,气体逸出,水被蒸发,符合质量守恒定律,故B不适合;
C、高锰酸钾受热分解的总质量,就等于生成的锰酸钾、二氧化锰和氧气的总质量,故C适合;
D、根据化学方程式可知,12g碳和16g氧气反应,碳有剩余,不能生成28g二氧化碳.故D不适合.
故选C.
点评:本题考查学生运用质量守恒定律分析推断的能力.
分析:根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变.
解答:A、镁条燃烧,是镁与氧气反应的过程,故它燃烧后生成物的质量比镁条的质量多出了参与反应的氧气的质量,故A不适合;
B、蜡烛燃烧时逐渐变短,是因为生成了二氧化碳和水,气体逸出,水被蒸发,符合质量守恒定律,故B不适合;
C、高锰酸钾受热分解的总质量,就等于生成的锰酸钾、二氧化锰和氧气的总质量,故C适合;
D、根据化学方程式可知,12g碳和16g氧气反应,碳有剩余,不能生成28g二氧化碳.故D不适合.
故选C.
点评:本题考查学生运用质量守恒定律分析推断的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 26、2009年4月22日是“世界水日”.水与人类的生活和生产密切相关.请回答以下问题:
26、2009年4月22日是“世界水日”.水与人类的生活和生产密切相关.请回答以下问题: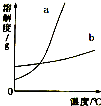 KNO3和KCl在不同温度时的溶解度如下表所示.请回答下列问题:
KNO3和KCl在不同温度时的溶解度如下表所示.请回答下列问题: