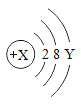题目内容
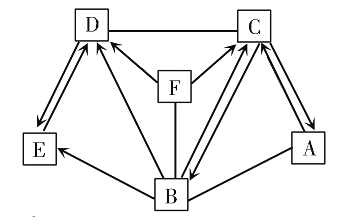
【题目】工业上有如图工艺流程: (石灰石中的杂质高温不分解且不溶于水)试回答:
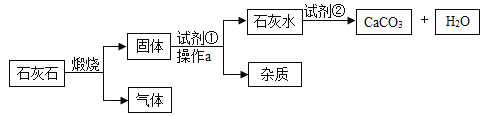
(1)煅烧石灰石发生反应的化学方程式:____________________。
(2)加入试剂①该反应的化学方程式:____________。操作a的名称是_____________实验室中进行此操作时,用到的玻璃仪器除玻璃棒、烧杯外,还需要______________。
(3)生产过程中,为了节约成本,会把有用的产物重新循环利用,该工艺可循环使用的物质是____ ( 填化学式) ,加入试剂②得到不溶于水的白色沉淀,其反应原理(用化学方程式表示)_______________。此工艺最后得到的碳酸钙和原石灰石的不同点是______________
【答案】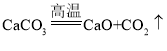
![]() 过滤 漏斗 H2O、CO2
过滤 漏斗 H2O、CO2 ![]() 生成的碳酸钙是纯净物,石灰石是混合物
生成的碳酸钙是纯净物,石灰石是混合物
【解析】
(1)石灰石主要成分是碳酸钙,煅烧石灰石发生反应的化学方程式为: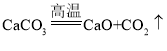 。
。
(2)碳酸钙发生化学反应生成氧化钙、二氧化碳,氧化钙与水反应生成氢氧化钙,故加入的试剂①是水,该反应的化学方程式:CaO+H2O=Ca(OH)2。通过过滤可将难溶于水的固体物质与液体分离,故操作a的名称是过滤,实验室中进行此操作时,用到的玻璃仪器除玻璃棒、烧杯外,还需要漏斗。
(3)生产过程中,H2O、CO2既是反应物又是生成物,故该工艺可循环使用的物质是H2O、CO2,加入试剂②得到不溶于水的白色沉淀,其反应原理是:CO2+Ca(OH)2=CaCO3↓+H2O。此工艺最后得到的碳酸钙和原石灰石的不同点是生成的碳酸钙是纯净物,石灰石是混合物。

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案【题目】在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如表所示,下列说法不正确的是( )
物质 | X | Y | Z | W |
反应前质量/g | 10 | 3 | 90 | 0 |
反应后质量/g | 3.2 | 3 | 待测 | 3.2 |
A. W可能是单质 B. Y可能是催化剂
C. 该反应是分解反应 D. 反应后Z物质的质量为![]()
【题目】某化学兴趣小组在研究燃烧时进行了如下探究。
(1)用下图装置进行实验(夹持仪器略去)。加热b处、c处的正中间,一-段时间后,b处火柴头燃烧,而a处火柴头和c处火柴梗均不燃烧。能验证“可燃物燃烧温度需要达到着火点”的现象是___________________ (填序号)。
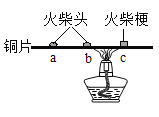
Aa处火柴头不燃烧,b处火柴头燃烧
Ba处火柴头不燃烧,c处火柴梗不燃烧
Cb处火柴头燃烧,c 处火柴梗不燃烧
(2)该小组同学发现铁丝燃烧没有火焰,蜡烛燃烧却有明亮的火焰。
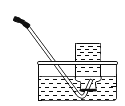
①点燃蜡烛,将金属导管一端伸入内焰,导出其中的物质,在另一端管口点燃,也有火焰产生(如图所示)。由此可知:蜡烛燃烧产生的火焰是由________________(填“固态”或“液态”或“气态”)物质燃烧形成的。
②查阅下表的资料可知:物质燃烧能否产生火焰与其________________(填“熔点”或“沸点”)和燃烧时温度有关。由此推测:钠在燃烧时,________________ (填 “有”或“没有”)火焰产生,其理由是___________________________。
物质 | 熔点/°C | 沸点/°C | 燃烧时温度/°C |
石蜡 | 50~70 | 300~ 550 | 约600 |
铁 | 1535 | 2750 | 约1800 |
钠 | 97.8 | 883 | 约1400 |