题目内容
【题目】根据下列图示回答有关问题:
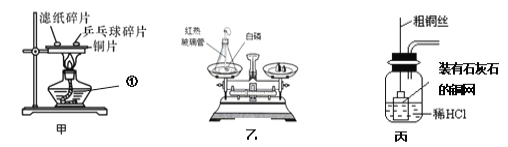
(1)实验甲中仪器①的名称是_____,该实验探究的燃烧条件是_____。
(2)实验乙的目的是_____,充分反应后,最后天平的指针应该_____(填“偏左”、“指向中央”或“偏右”)。
(3)实验丙中制取二氧化碳的装置优点是_____,若将铜丝和铜网改为铁丝和铁网是否可行?_____(填“可行”或“不可行”),请用化学方程式表示其原因_____。
【答案】酒精灯 温度需达到可燃物的着火点 )验证质量守恒定律 指向中央 便于随时控制反应的发生与停止 不可行 Fe+2HCl=FeCl2+H2↑
【解析】
(1)根据仪器的名称、实验现象来分析解答;
(2)根据实验装置以及反应的原理来分析;
(3)根据装置的特点、金属的性质、化学反应的原理来分析。
(1)仪器①是酒精灯;在实验中可以看到,放在薄铜片上的乒乓球碎片和滤纸碎片,先燃烧起来的是乒乓球碎片,这个现象说明燃烧的条件之一是温度需要达到可燃物的着火点;故填:酒精灯;温度需达到可燃物的着火点;
(2)该实验是验证质量守恒定律,该装置是一个密封装置,所以反应后天平仍然平衡,即天平的指针应该指向中央;故填:验证质量守恒定律;指向中央;
(3)该装置的优点是便于随时控制反应的发生与停止;在实验室中用大理石(或石灰石)和稀盐酸制取二氧化碳,不能将实验中的铜网换成铁网,是因为铁能够和稀盐酸反应生成氢气,使制得的二氧化碳气体中混有氢气;故填:便于随时控制反应的发生与停止;不可行;Fe+2HCl=FeCl2+H2↑

【题目】某研究小组探究![]() 质量分数、溶液pH、温度对反应速率的影响,进行如下实验:
质量分数、溶液pH、温度对反应速率的影响,进行如下实验:
实验一、设计如下表实验方案:
实验序号 |
| pH | 温度 | 每分钟气泡数 |
1 | 30 | 5 | 20 | |
2 | 30 | 6 | 20 | |
3 | 30 | 11 | 20 | |
4 | 15 | 11 | 30 | |
5 | a | 11 | b |
![]() 实验
实验![]() 的实验目的是______。
的实验目的是______。
![]() 在实验5中,若
在实验5中,若![]() ,则
,则![]() ______。
______。
实验二、探究制取氧气的适宜催化剂,实验方案如下:
I.用![]() 、CuO、
、CuO、![]() 、
、![]() 四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用。
四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用。
![]() 取30粒含
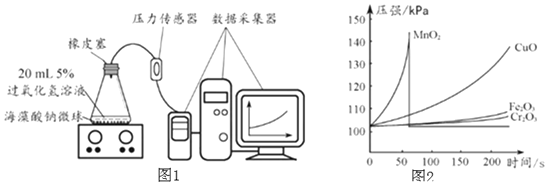
取30粒含![]() 的海藻酸钠微球,采用图1所示装置进行实验。改用其他三种微球,分别重复上述实验,得到图2的锥形瓶内压强随时间变化的曲线图。
的海藻酸钠微球,采用图1所示装置进行实验。改用其他三种微球,分别重复上述实验,得到图2的锥形瓶内压强随时间变化的曲线图。
![]() 每次实验时,海藻酸钠微球数应相同的原因______。
每次实验时,海藻酸钠微球数应相同的原因______。
![]() 从实验曲线看,催化效果较好、反应温和的催化剂是______。
从实验曲线看,催化效果较好、反应温和的催化剂是______。
【题目】铁与水蒸气在高温条件下反应生成一种铁的氧化物和一种气体单质,实验装置如图所示。

(1)试管尾部放一团湿棉花的目的是_____。
(2)用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到上方空中,说明生成的气体是_____。
(3)探究试管中剩余固体成分。
(查阅资料)①几种常见铁的氧化物的颜色、状态及能否被磁铁吸引如下表所示。
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
②四氧化三铁能与稀硫酸反应:Fe3O4+4H2SO4=FeSO4+Fe2(SO4)3+4H2O
(初步实验验证)试管中剩余固体为黑色,能全部被磁铁吸引,则剩余固体一定不含的铁的氧化物是_____、_____ 。
(猜想与假设)猜想一:剩余固体是Fe3O4;猜想二:剩余固体是_____ 。
(继续进行实验)
实验操作 | 实验现象 | 实验结论 |
取少量黑色固体于试管中,滴加足量的稀硫酸。 | _____ | 猜想二成立。 |
(实验结论)铁和水蒸气反应的化学方程式为_____。
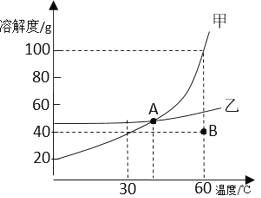
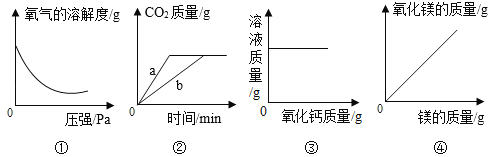
【题目】下列图像不能正确反映其对应关系的是
|
|
|
|
A.表示将一定量60 ℃硝酸钾饱和溶液冷却至室温 | B.t ℃,向一定量的饱和石灰水中加入少量生石灰 | C.将水通电一段时间 | D.向两份完全相同的盐酸中,分别加Cu(OH)2和CuO |
A. AB. BC. CD. D
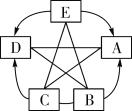
【题目】如图A、B分别是镁元素、硫元素在元素周期表中的信息,C、D、E是三种粒子的结构示意图,表格是元素周期表的一部分,

H | He | ||||||
C | ① | ||||||
Al | ② | ③ | |||||
(1)C、D、E中与A属于同种元素的微粒是_____;
(2)B与元素周期表中_____(填①或②或③)的化学性质相似;
(3)D微粒的符号为_____;
(4)元素②的核外有_____个电子层。