题目内容
某实验室中需要1.6g氧气进行实验.若用加热氯酸钾(在催化剂MnO2存在下)的方法制取这些氧气;(1)需消耗氯酸钾的质量是多少?
(2)同时可得到氯化钾的质量是多少?
【答案】分析:氯酸钾分解产生了氧气,题给了氧气的质量,故可以根据氧气的质量结合化学方程式来求算氯酸钾和氯化钾的质量.
解答:解:设需要氯酸钾的质量为x
2KCl03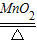 2KCl+3O2↑
2KCl+3O2↑
245 96
x 1.6 g
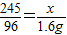
解得:x≈4.08g
根据质量守恒定律可知生成氯化钾的质量为4.08g-1.6g=2.48g
答:(1)需消耗氯酸钾的质量是4.08g;(2)同时可得到氯化钾的质量是2.48g;
点评:在利用反应的化学方程式进行计算时,首先要正确书写化学方程式,正确书写化学方程式要遵循两个原则:以客观事实为基础,遵守质量守恒定律;此外,还要注意:解、设、列、答要完整,已知物质与未知物质的质量关系及比例式要正确写出,计算过程中要带单位进行,设未知物质量时不需要单位等.
解答:解:设需要氯酸钾的质量为x
2KCl03
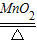 2KCl+3O2↑
2KCl+3O2↑245 96
x 1.6 g
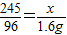
解得:x≈4.08g
根据质量守恒定律可知生成氯化钾的质量为4.08g-1.6g=2.48g
答:(1)需消耗氯酸钾的质量是4.08g;(2)同时可得到氯化钾的质量是2.48g;
点评:在利用反应的化学方程式进行计算时,首先要正确书写化学方程式,正确书写化学方程式要遵循两个原则:以客观事实为基础,遵守质量守恒定律;此外,还要注意:解、设、列、答要完整,已知物质与未知物质的质量关系及比例式要正确写出,计算过程中要带单位进行,设未知物质量时不需要单位等.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
 (2013?塘沽区二模)某化学学习小组同学在实验室中练习配制一定溶质质量分数的溶液.
(2013?塘沽区二模)某化学学习小组同学在实验室中练习配制一定溶质质量分数的溶液. ,若X等于11,则该微粒表示
,若X等于11,则该微粒表示