题目内容
吸烟有害健康,香烟中对人体危害最大的是尼古丁,其化学式为C10H14N2,它是由 种元素组成,每个分子中含有 个原子;尼古丁中碳、氢、氮元素的质量比为 .
考点:化学式的书写及意义,元素质量比的计算
专题:化学用语和质量守恒定律
分析:根据尼古丁化学式的含义,化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答:解:由C10H14N2可知,尼古丁是由碳、氢和氮三种元素组成的;1个尼古丁分子是由10个碳原子、14个氢原子、2个氮原子构成的,则每个尼古丁分子中共含有26个原子.
碳元素、氢元素、氮元素的质量比为:(12×10):(1×14):(14×2)=60:7:14.故填:三;26;60:7:14.
碳元素、氢元素、氮元素的质量比为:(12×10):(1×14):(14×2)=60:7:14.故填:三;26;60:7:14.
点评:解答本题要充分理解化学式的含义,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 集气瓶被誉为“万能瓶”,如图装置是其中的一种.当被收集的气体从a口进入时,瓶内空气从b口排出,相当于向上排空法.现若将被收集的气体从b口进入,则它可收集的气体为( )(CO2密度大于空气;CH4、H2密度小于空气)
集气瓶被誉为“万能瓶”,如图装置是其中的一种.当被收集的气体从a口进入时,瓶内空气从b口排出,相当于向上排空法.现若将被收集的气体从b口进入,则它可收集的气体为( )(CO2密度大于空气;CH4、H2密度小于空气)①H2②CH4③CO2④O2.
| A、①③④ | B、②③④ |
| C、①② | D、①②③④ |
下列实验操作不正确的是( )
A、 添加酒精 |
B、 蒸发食盐水 |
C、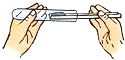 取用粉末状药品 取用粉末状药品 |
D、 氧气验满 |
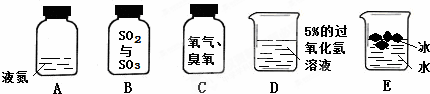
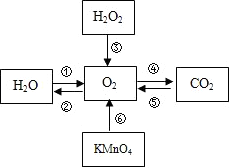 构建知识网络是一种重要的学习方法.下图是某同学构建的有关氧气获得和性质的网络图.请根据右图回答有关问题:
构建知识网络是一种重要的学习方法.下图是某同学构建的有关氧气获得和性质的网络图.请根据右图回答有关问题: