题目内容
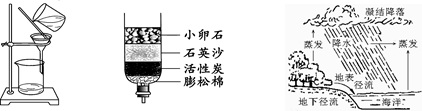
小明同学去黄山旅游时,用瓶装了一些山下的泉水,带回实验室在老师的指导下,按下列流程进行实验,制取蒸馏水。
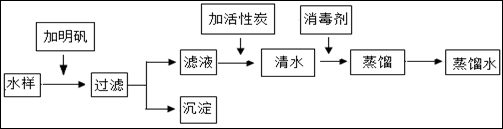
请回答下列问题:
(1)在水样中加入明矾的作用是 。
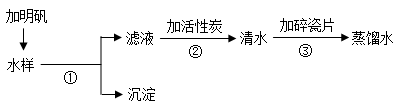
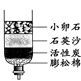
(2)进行过滤操作时,下列做法错误的是 。
A.玻璃棒靠在滤纸边缘的任一下方 B.漏斗下端的管口要紧靠烧杯的内壁
C.滤纸的边缘要低于漏斗口 D.液面要低于滤纸边缘
(3)向滤液中加入活性炭,利用其 性,除去水样中的色素和异味。
(4)高铁酸钠(Na2FeO4)是一种常用的消毒剂,目前被广泛应用于自来水净化。高铁酸钠中铁元素的化合价为 。
(5)以下方法得到的水,其纯度最高的是 。
A.过滤 B.吸附 C.沉淀 D.蒸馏
(6)认真观察右图A、B两装置,写出B装置中发

生反应的化学方程式 ;
用分子和原子的观点分析比较A装置和B装
置在试验过程中水的变化情况 。

请回答下列问题:
(1)在水样中加入明矾的作用是 。
(2)进行过滤操作时,下列做法错误的是 。
A.玻璃棒靠在滤纸边缘的任一下方 B.漏斗下端的管口要紧靠烧杯的内壁
C.滤纸的边缘要低于漏斗口 D.液面要低于滤纸边缘
(3)向滤液中加入活性炭,利用其 性,除去水样中的色素和异味。
(4)高铁酸钠(Na2FeO4)是一种常用的消毒剂,目前被广泛应用于自来水净化。高铁酸钠中铁元素的化合价为 。
(5)以下方法得到的水,其纯度最高的是 。
A.过滤 B.吸附 C.沉淀 D.蒸馏
(6)认真观察右图A、B两装置,写出B装置中发

生反应的化学方程式 ;
用分子和原子的观点分析比较A装置和B装
置在试验过程中水的变化情况 。
(1)使水中小颗粒凝聚成大颗粒(或起凝聚作用) (2)A
(3)吸附 (4)+6 (5)D
(6)2H2O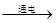 2 H2↑+O2↑
2 H2↑+O2↑
A中的水分子本身没有改变,改变的是分子之间的间隔;B中的水分子发生了改变,变成了氢分子和氧分子(共1分)
(3)吸附 (4)+6 (5)D
(6)2H2O
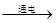 2 H2↑+O2↑
2 H2↑+O2↑ A中的水分子本身没有改变,改变的是分子之间的间隔;B中的水分子发生了改变,变成了氢分子和氧分子(共1分)
分析:题目考查了水的净化以及过滤操作的操作要领,同时结合净水剂考查化合价的规则的运用,从微观分析物理变化与化学变化.
解答:解:(1)在水样中加入明矾的作用,是利用明矾在水中形成胶体后,吸附凝聚小颗粒而沉淀.故答案为:使水中小颗粒凝聚成大颗粒(或起凝聚作用)
(2)A.玻璃棒紧靠三层滤纸处,而不是任一下方.错误;
B.漏斗下端的管口要紧靠烧杯的内壁,这样能够防止迸溅和加快过滤速度.正确;
C.滤纸的边缘要低于漏斗口,这样能够使滤纸不容易破损.正确;
D.液面要低于滤纸边缘,这样能够使滤液被充分过滤.正确.
故选A.
(3)活性炭具有疏松多孔的结构,能够吸附有色物质和异味.所以向滤液中加入活性炭,利用其吸附性,除去水样中的色素和异味.故填:吸附.
(4)高铁酸钠(Na2FeO4),由于钠元素为+1价,氧元素为-2价,根据化合价代数和为零,可得铁元素为+6价.故填:+6.
(5)A.过滤,是除去不溶性颗粒的过程,不能去除可溶性杂质;
B.吸附,有明矾吸附和活性炭吸附,两者都不能除去水中可溶性杂质;
C.沉淀,是自然沉降的方式,除去的是大颗粒的物质,小颗粒以及可溶性物质无法去除;
D.蒸馏,是水受热成水蒸气后再次冷凝的过程,这样得到的水几乎就是纯净物.
故选D.
(6)图A是简易蒸馏水的制造过程,是物理变化,而图B是电解水的过程,是化学变化.故答案为:2H2O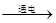 2H2↑+O2↑; A中的水分子本身没有改变,改变的是分子之间的间隔;B中的水分子发生了改变,变成了氢分子和氧分子
2H2↑+O2↑; A中的水分子本身没有改变,改变的是分子之间的间隔;B中的水分子发生了改变,变成了氢分子和氧分子
解答:解:(1)在水样中加入明矾的作用,是利用明矾在水中形成胶体后,吸附凝聚小颗粒而沉淀.故答案为:使水中小颗粒凝聚成大颗粒(或起凝聚作用)
(2)A.玻璃棒紧靠三层滤纸处,而不是任一下方.错误;
B.漏斗下端的管口要紧靠烧杯的内壁,这样能够防止迸溅和加快过滤速度.正确;
C.滤纸的边缘要低于漏斗口,这样能够使滤纸不容易破损.正确;
D.液面要低于滤纸边缘,这样能够使滤液被充分过滤.正确.
故选A.
(3)活性炭具有疏松多孔的结构,能够吸附有色物质和异味.所以向滤液中加入活性炭,利用其吸附性,除去水样中的色素和异味.故填:吸附.
(4)高铁酸钠(Na2FeO4),由于钠元素为+1价,氧元素为-2价,根据化合价代数和为零,可得铁元素为+6价.故填:+6.
(5)A.过滤,是除去不溶性颗粒的过程,不能去除可溶性杂质;
B.吸附,有明矾吸附和活性炭吸附,两者都不能除去水中可溶性杂质;
C.沉淀,是自然沉降的方式,除去的是大颗粒的物质,小颗粒以及可溶性物质无法去除;
D.蒸馏,是水受热成水蒸气后再次冷凝的过程,这样得到的水几乎就是纯净物.
故选D.
(6)图A是简易蒸馏水的制造过程,是物理变化,而图B是电解水的过程,是化学变化.故答案为:2H2O
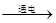 2H2↑+O2↑; A中的水分子本身没有改变,改变的是分子之间的间隔;B中的水分子发生了改变,变成了氢分子和氧分子
2H2↑+O2↑; A中的水分子本身没有改变,改变的是分子之间的间隔;B中的水分子发生了改变,变成了氢分子和氧分子
练习册系列答案
相关题目