题目内容
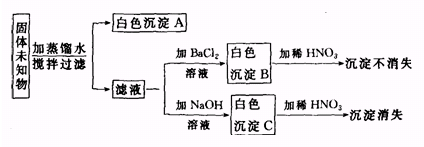
(1)根据上述实验现象可以肯定白色固体中一定含有
(2)写出生成B和C的化学反应方程式:
(2)生成B的反应是氯化钡和硫酸钠溶液反应生成硫酸钡沉淀和氯化钠,化学反应方程式为BaCl2+Na2SO4═BaSO4↓+2NaCl;生成C的反应是氢氧化钠溶液和氯化镁溶液反应生成氢氧化镁沉淀和氯化钠,化学反应方程式为MgCl2+2NaOH═Mg(OH)2↓+2NaCl.故填:BaCl2+Na2SO4═BaSO4↓+2NaCl;MgCl2+2NaOH═Mg(OH)2↓+2NaCl.

某白色固体粉末可能含有CuSO4、BaCl2、NaOH、Na2CO3中的一种或几种.某化学小组进行了如下实验:①取一定量白色粉末,加入足量水,振荡,得到无色透明溶液;②取少量①的溶液,加入足量盐酸,有气泡产生.下列对固体粉末成分的判断中,不正确的是( )
|
| A. | 一定无CuSO4 | B. | 一定有Na2CO3 | C. | 可能有NaOH | D. | 可能有BaCl2 |
某些食品的包装袋内,放有装有白色颗粒状固体的小纸袋,上面写着“干燥剂,主要成分为生石灰”。某同学对一袋久置空气中的干燥剂进行了探究。
他先取部分久置干燥剂倒入适量水中,充分搅拌、过滤,得到白色固体和滤液。然后对滤液的酸碱性和白色固体的组成作了探究。
【实验探究一】探究滤液的酸碱性
该同学测定了滤液的酸碱性,你认为该滤液显 (填“酸性”“碱性”或“中性”)。
【实验探究二】探究白色固体的组成
该同学认为白色固体中可能含有的物质是CaO、Ca(OH)2、CaCO3。
他查阅有关资料得知:
CaO是一种白色固体,俗称生石灰,能与水反应生成氢氧化钙,并放出热量。氢氧化钙微溶于水。
【分析判断】你认为该白色固体中一定不含有的物质是 。
【实验操作】下面是该同学设计的进一步探究白色固体组成的实验方案,请你和他一起完成实验报告。
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量白色固体,倒入适量水,充分搅拌、静置; ②向上层清液中滴加无色酚酞溶液 | 上层清液呈 现 色 | 白色固体中一定含有氢氧 |
| 另取少量白色固体放入试管中,滴加稀盐酸 | _________ | 白色固体中一定含有碳酸钙 |
【总结反思】
(1)只通过以上实验,还不能证明这袋久置于空气中的干燥剂中是否含有CaO。请用化学方程式表示原因 。
(2)请你简述一个证明这袋干燥剂中含有较多量CaO的简易实验: 。
 化钙
化钙