题目内容
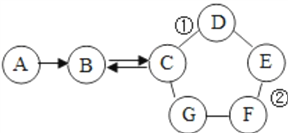
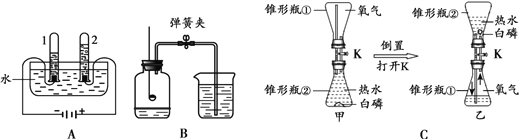
【题目】下列A→D的实验装置进行合理组合,即可制取二氧化碳气体也可制取氧气。

(1)写出标注①的仪器名称:__________。
(2)实验室用A装置制取氧气时,在分液漏斗中添加的药品是_________(填化学式),用排水法收集氧气,观察到_______时,再将注满水的集气瓶倒扣住导气管,收集氧气。若用加热分解高锰酸钾的方法制取氧气,则选用的发生装置为______(填标号),该反应的化学方程式为_____________。
(3)用A、D装置制取并收集二氧化碳,仪器接口的连接顺序是a→___(填“b”或“c”)。若在D中装半瓶氢氧化钠溶液,将A中生成的二氧化碳气体通入其中一会儿,肉眼观察不到什么可见现象。实验小组将进行如下三个实验探究活动。用实验的方法证明二氧化碳与氢氧化钠发生了反应,并验证产物碳酸钠。
实验一:取反应后的D中溶液,滴加酚酞试剂,溶液变红。
实验二:取反应后的D中溶液,加几滴稀盐酸,未观察到气泡的产生。
实验三:取反应后的D中溶液,滴加澄清石灰水,出现浑浊。
(4)研究表明,实验一不能证明化学反应是否进行,理由是___________________。
(5)请判断实验二能否证明变化中无碳酸钠生成并说明理由___________________。
(6)写出实验三发生变化的化学反应方程式_________________________________。
查资料:常温下,氢氧化钠易溶于酒精溶剂形成溶液,而碳酸钠难溶于酒精溶剂。
(7)请你根据“资料”信息,设计一个实验方案,证明二氧化碳与氢氧化钠发生了化学的反应:____________________________________________________________。
(8)若以上方案有人用75%的医用酒精来配制氢氧化钠溶液进行实验,结果达不到预期效果,原因是________________________________________________________。
【答案】 酒精灯 H2O2 气泡连续均匀放出 B 2KMnO4 △ K2MnO4+ MnO2+O2↑ c 氢氧化钠和碳酸钠溶液都呈碱性 不能,反应后D中溶液氢氧化钠过量,会与稀盐酸反应 Ca(OH)2 + Na2CO3 = CaCO3↓ + 2NaOH 将二氧化碳通入氢氧化钠酒精溶液中,能观察到有不溶性物质生成 75%的酒精溶液中含有水,碳酸钠会溶于水
【解析】(1)由图可知,①是酒精灯;(2)A装置属固液在常温下反应的装置,故是用过氧化氢和二氧化锰制取氧气,其中二氧化锰从锥形瓶中加入,过氧化氢从分液漏斗中加入;用排水法收集氧气时,要等气泡连续且均匀冒出时开始收集,否则会导致收集的氧气不纯;用加热分解高锰酸钾的方法制取氧气,属固固加热型,选B装置;在加热的条件下,高锰酸钾分解生成锰酸钾、二氧化锰和氧气,反应的化学方程式表示为2KMnO4 △ K2MnO4+ MnO2+O2↑;(3)二氧化碳的密度比空气大,会先聚集在集气瓶的底部然后上升,故二氧化碳应从c端通入;(4)氢氧化钠和二氧化碳反应生成碳酸钠,氢氧化钠和碳酸钠均呈碱性,故无色酚酞变红不能说二氧化碳与氢氧化钠发生了反应;(5)若D溶液中含有氢氧化钠,滴入的稀盐酸先与氢氧化钠溶液反应,也可能观察不到气泡;(6)氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式表示为Ca(OH)2 + Na2CO3 = CaCO3↓ + 2NaOH;(7)根据资料可将将二氧化碳通入氢氧化钠酒精溶液中,若能观察到有不溶性物质生成,说明氢氧化钠和二氧化碳发生反应生成了碳酸钠;(8)由于75%的酒精溶液中含有水,而碳酸钠会溶于水,故果达不到预期效果。

 阅读快车系列答案
阅读快车系列答案