题目内容
【题目】两个烧杯中装有等质量的金属锌和镁,然后分别逐渐加入同浓度的稀硫酸,产生氢气的质量与加入硫酸的质量关系如图所示。下列说法正确的是( )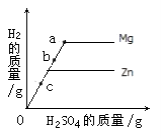
A.a点时,两个烧杯中的酸都恰好完全反应
B.b点时,两个烧杯中产生氢气的质量相同
C.c点时,两个烧杯中都有金属剩余
D.该图反映出镁比锌的金属活动性强
【答案】C
【解析】A 氢气的质量达到最多时,金属完全反应。完全反应a点时,镁与稀硫酸恰好完全反应,锌早已完全反应;A不符合题意;
B、b点时,镁产生的氢气多,锌产生的氢气质量少;B不符合题意;
C、c点时,锌与镁均均还没有完全反应,两个烧杯中都有金属剩余;C符合题意;
D、由产生氢气的质量与加入硫酸的质量关系图,镁产生的氢气质量多,但无法得出镁与锌的金属活动性的关系;D不符合题意.
故答案为:C.镁、锌金属活动性均比氢强,均能与稀硫酸反应生成氢气,等质量的金属锌和镁,分别逐渐加入同浓度的稀硫酸,由生氢气的质量与加入硫酸的质量关系图,最终镁产生的氢气质量多.

练习册系列答案
相关题目