题目内容
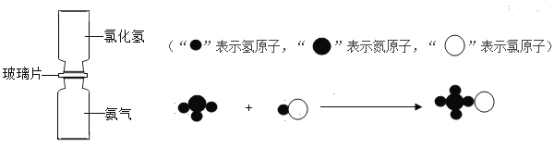
【题目】下列关于N2 + O2 ![]() 2NO的说法中,正确的是
2NO的说法中,正确的是
A.反应后原子种类减少
B.表示氮气加氧气等于一氧化氮
C.通过化学方程式可以知道参加反应的物质微粒个数比
D.要想求出生成的NO的质量,必须同时知道参加反应的N2和O2 的质量
【答案】C
【解析】
A、根据化学方程式可知,反应后原子种类不变,故A错误;
B、该化学方程表示氮气与氧气在放电条件下生成一氧化氮,故B错误;
C、化学方程式中化学式前计量数之比等于参加反应的物质微粒个数比,通过化学方程式可以知道参加反应的物质微粒个数比,故C正确;
D、要想求出生成的NO的质量,不一定必须同时知道参加反应的N2和O2 的质量,可根据反应中各物质的质量比以及N2和O2其中任意一种的质量求出NO的质量,故D错误。故选C。

【题目】如图所示装置可用于测定空气中氧气的含量。下列说法不正确的是
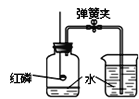
A.不能用木炭代替红磷
B.燃烧匙中盛放过量的红磷
C.通过实验可以得出空气中氮气与氧气的体积比约为5∶1
D.燃烧结束后不能立刻打开弹簧夹
【题目】“二氧化碳的实验室制法”是九年级化学八个基础实验之一,某小组在老师的指导下进行了一系列探究实验。请你一起参与他们的活动,并回答相关问题。
[探究活动一]:探究二氧化碳的制取原理
(1)选用药品。
按下表进行实验,取等质量的大理石加人足量酸中(杂质不与酸反应),产生二氧化碳体积随时间变化曲线如图1所示:
实验编号 | 药品 |
Ⅰ | 块状大理石、10%盐酸溶液 |
Ⅱ | 块状大理石、10%硫酸溶液 |
Ⅲ | 大理石粉末、10%盐酸溶液 |
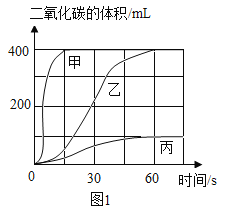
查阅资料:氯化钙易溶于水,硫酸钙微溶于水确定用乙对应的药品制备二氧化碳,相应的化学方程式是________;不用甲对应的药品,理由是______________;图中丙反应产生二氧化碳的量明显偏小的原因可能是_________。
(2)搭建装置。
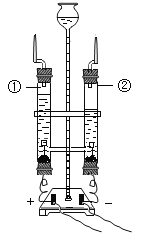
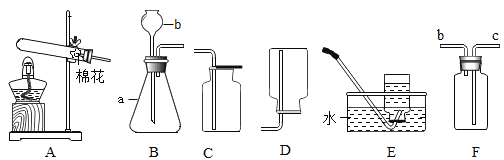
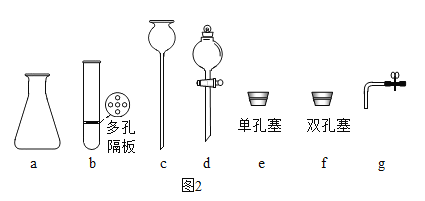
如果组装一套可控制反应发生和停止的装置,应选用图2中的______________________(选填编号)。
[探究活动二]:探究能否用排水法收集二氧化碳
实验一:同学们利用图3装置分别用排气法和排水法收集一瓶二氧化碳
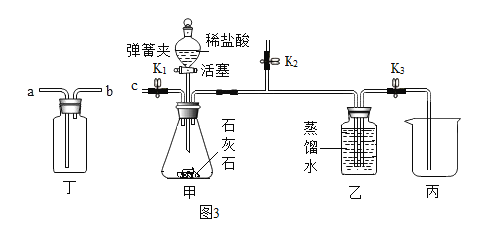
(3)实验前需先将甲装置中的空气排尽。其操作是:关闭弹簧夹K1和_______________________;开启弹簧夹_______________________。,打开活塞,滴加稀盐酸至空气排尽。检验空气已排尽的方法是_______________________;
(4)将丁与甲相连,可以用排气法收集二氧化碳气体,管口连接顺序是c与____相连。
排水法收集气体:关闭K1、K2,打开K3,滴入稀盐酸并开始计时,待水排尽,用时28秒。
排气法收集气体:关闭K2、K3,打开K1,滴入稀盐酸并开始计时,待空气排尽,用时15秒。
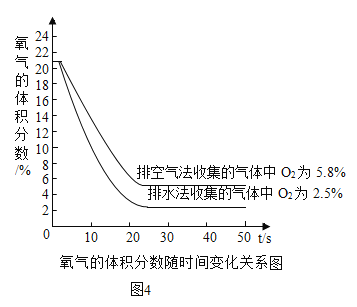
实验二:用氧气传感器分别测定排空气法和排水法收集的两瓶二氧化碳气体中氧气的体积分数(图4)。
[结论反思]
两种方法收集二氧化碳气体中的氧气均来自于空气,如果以氧气占空气体积的1/5计算,则:
(5)两种方法收集的气体中二氧化碳体积分数的差值是_______________________;
(6)根据图中数据判断下列说法正确的是________________________(填字母)。
A 排空气法验满时,若瓶口木条熄灭,则瓶中二氧化碳体积分数为100%
B 图中用排空气法收集的气体中二氧化碳的体积分数为94.2%
C 图中用排水法收集的气体中二氧化碳的体积分数为87.5%
D 从图中数据可推测二氧化碳从水里逸出的速度远大于溶解在水里的速度
(7)根据上述实验分析你认为_______________________(填“ 能”或“不能”)用排水法收集二氧化碳。
【题目】请根据下表回答有关问题【除第(1)、(5)外,其余各小题均用序号填空】
(1)写出下列或其有效成分的化学式火碱________;生石灰___________熟石灰_______
(2)表中物质属于氧化物的是:______;属于盐的是:_______ ;
序号 | ① | ② | ③ | ④ |
物质 | 醋酸 | 生石灰 | 熟石灰 | 碳酸钠 |
化学式 | CH3COOH |
(3)上述四种物质放入相等的水中,所得的溶液中pH最小的是________ ;
(4)你认为CH3COOH(其性质类似于盐酸)可以与表中________物质发生化学反应;
(5)利用表中作反应物(可以加水或与在水中进行),写出符合下列要求的化学方程式
Ⅰ 生石灰转化为熟石灰:___________________________;
Ⅱ 制取氢氧化钠: ________________________________。