题目内容
水蒸气通过炽热的煤所产生的混合气体主要成分是CO、H2,其中混有CO2和水蒸气.请用下列装置设计一个实验,来确认上述混合气体中含有CO和H2(假设每步反应均完全反应).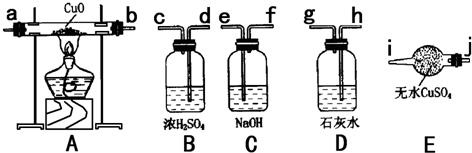
(查资料知:硫酸铜未白色固体,遇水变为蓝色固体)
(1)连接上述装置的正确顺序是(按气流从左向右的顺序):
ef→
(2)装置A中的实验现象是:
(3)装置D中实验现象是:
(4)装置B的作用是
分析:(1)检验气体时,先排除干扰.注意干燥、洗气、检验气体时,气体从“长管进,短管出”.
(2)根据装置A中发生的反应解答;
(3)二氧化碳能使石灰水变浑浊;
(4)浓硫酸具有吸水性,无水硫酸铜遇水变为蓝色固体.
(2)根据装置A中发生的反应解答;
(3)二氧化碳能使石灰水变浑浊;
(4)浓硫酸具有吸水性,无水硫酸铜遇水变为蓝色固体.
解答:解:(1)为了验证混合气中含有CO和H2,实验仪器的连接先后顺序为:除二氧化碳→除掉水分→还原装置→检验水分→检验二氧化碳;除杂质连接仪器的原则是:长进短出;
(2)装置A中的氧化铜被氢气和一氧化碳还原,反应实验现象是黑色粉末变成红色,反应方程式为:H2+CuO
Cu+H2O,CO+CuO
Cu+CO2;
(3)由于一氧化碳能还原氧化铜,使黑色粉末变成红色,并能生成二氧化碳,使澄清石灰水变浑浊;
(4)浓硫酸有吸水性,故装置B的作用是吸收水蒸气,无水硫酸铜遇水变蓝,故装置E的作用是检验是否有水生成;
故答案为:(1)dc(2)黑色粉末变成红色,H2+CuO
Cu+H2O,CO+CuO
Cu+CO2;
(3)溶液变浑浊,CO2+Ca(OH)2═CaCO3↓+H2O;
(4)吸收水蒸气,检验是否有水生成.
(2)装置A中的氧化铜被氢气和一氧化碳还原,反应实验现象是黑色粉末变成红色,反应方程式为:H2+CuO
| ||
| ||
(3)由于一氧化碳能还原氧化铜,使黑色粉末变成红色,并能生成二氧化碳,使澄清石灰水变浑浊;
(4)浓硫酸有吸水性,故装置B的作用是吸收水蒸气,无水硫酸铜遇水变蓝,故装置E的作用是检验是否有水生成;
故答案为:(1)dc(2)黑色粉末变成红色,H2+CuO
| ||
| ||
(3)溶液变浑浊,CO2+Ca(OH)2═CaCO3↓+H2O;
(4)吸收水蒸气,检验是否有水生成.
点评:通过回答本题要知道除杂质时要把水放到最后除去,如果验证水的存在时要把验证水存在的无水硫酸铜放在最前面.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
 Cu+CO2
Cu+CO2