题目内容
【题目】实验室配制100g 10%的氯化钠溶液,有关实验操作不正确的是( )
A.用托盘天平称取10.0g氯化钠
B.用量筒量取90.0mL 的水
C.将称取的氯化钠倒入量筒中溶解
D.将配制的溶液装入试剂瓶中,贴上标签
【答案】C
【解析】解:A、溶质的质量=溶液的质量×溶质的质量分数,所以用托盘天平称取10.0g氯化钠,故A正确; B、根据溶剂的体积= ![]() ,所以用量筒量取90.0mL 的水,故B正确;
,所以用量筒量取90.0mL 的水,故B正确;
C、量筒不能用来配制溶液,应该放在烧杯内溶解,故C错误;
D、将配好的溶液装入试剂瓶中,塞好瓶塞并贴上标签,故D正确.
故选:C.
A、根据溶质的质量=溶液的质量×溶质的质量分数进行解答;
B、根据溶剂的体积= ![]() 进行解答;
进行解答;
C、根据量筒不能用来配制溶液进行解答;
D、根据溶液配制的步骤进行解答.

 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案【题目】碱式碳酸盐广泛应用于工农业生产.
(1)某碱式碳酸盐样品M(OH)2MCO3 , 为确定金属M的相对原子质量,某研究小组设计如下实验装置及步骤(不考虑植物油中溶解CO2产生的影响). 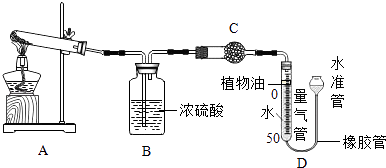
①连接装置并;②准确称量样品的质量;③装药品,调节量气装置两边液面相平,读数;④加热至样品质量不再减少;⑤冷却到室温;⑥调节量气装置两边液面相平,读数、列式计算.
Ⅰ、请将上述实验步骤补充完整.
Ⅱ、装置B的作用是 , 少量植物油的作用是 , C中的试剂是(填字母序号).
a、碱石灰 b、浓硫酸 c、硫酸铜
Ⅲ、步骤⑥中调节液面相平的操作是将水准管(填“缓慢上移”或“缓慢下移”).
Ⅳ、若其它操作均正确,仅因下列因素可使M相对原子质量的测定结果偏大的是(填字母序号).
a、反应前量气管水面到0刻度处,反应后仰视读数
b、样品未分解完全即停止实验
c、量气管中未加植物油
(2)实际生产中的碱式碳酸铜可表示为Cu(OH)2mCuCO3 , 某研究小组仍使用上述装置测定m的值,测得3组数据如下表所示.取3组数据的平均值得到CO2的体积为mL,又已知常温常压下CO2的密度为1.964g/L,据此计算m的值.(写出计算m的过程,最后结果保留小数点后两位)
组别 | 样品质量 | CO2的体积 |
第1组 | 0.21g | 22.39mL |
第2组 | 0.21g | 22.41mL |
第3组 | 0.21g | 22.40mL |