题目内容
Ag、Cu、Fe和Al是生产或生活中广泛使用的金属.
(1)四种金属中,不是银白色的是 .
(2)铁制品容易锈蚀,铁生锈的条件是 .生锈的废钢铁可回收重新冶炼,用一氧化碳还原氧化铁的化学方程式为 .
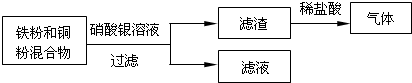
(3)根据如图所示回答:滤渣中一定有的金属是 ,滤渣与稀盐酸反应的化学方程式为 ;滤液中的溶质是 .
(1)四种金属中,不是银白色的是
(2)铁制品容易锈蚀,铁生锈的条件是
(3)根据如图所示回答:滤渣中一定有的金属是

分析:(1)四种金属中Cu不是银白色的;
(2)铁制品容易与水和氧气接触而生锈;用一氧化碳还原氧化铁的化学方程式为3CO+Fe2O3
2Fe+3CO2;
(3)由滤渣与盐酸反应放出气体,则滤渣中一定有Fe,还会有Cu、Ag;滤渣与稀盐酸反应的化学方程式为Fe+2HCl═FeCl2+H2↑;由于稀硝酸具有强氧化性,所以滤液中的溶质是Fe(NO3)2.
(2)铁制品容易与水和氧气接触而生锈;用一氧化碳还原氧化铁的化学方程式为3CO+Fe2O3
| ||
(3)由滤渣与盐酸反应放出气体,则滤渣中一定有Fe,还会有Cu、Ag;滤渣与稀盐酸反应的化学方程式为Fe+2HCl═FeCl2+H2↑;由于稀硝酸具有强氧化性,所以滤液中的溶质是Fe(NO3)2.
解答:解:(1)Ag、Cu、Fe和Al中,Cu是黑色金属,不是银白色的;
(2)铁制品容易锈蚀,铁生锈的条件是与水和氧气接触;生锈的废钢铁可回收重新冶炼,用一氧化碳还原氧化铁的化学方程式为3CO+Fe2O3
2Fe+3CO2;
(3)根据如图所示滤渣与盐酸反应放出气体,则滤渣中一定有Fe,Fe能把Cu、Ag置换出来,故滤渣中也一定有Cu、Ag;滤渣与稀盐酸反应的化学方程式为Fe+2HCl═FeCl2+H2↑;由于稀硝酸具有强氧化性,所以滤液中的溶质是Fe(NO3)2.
故答案为:(1)Cu
(2)与水和氧气接触;3CO+Fe2O3
2Fe+3CO2
(3)Fe、Cu、Ag;Fe+2HCl═FeCl2+H2↑;Fe(NO3)2
(2)铁制品容易锈蚀,铁生锈的条件是与水和氧气接触;生锈的废钢铁可回收重新冶炼,用一氧化碳还原氧化铁的化学方程式为3CO+Fe2O3
| ||
(3)根据如图所示滤渣与盐酸反应放出气体,则滤渣中一定有Fe,Fe能把Cu、Ag置换出来,故滤渣中也一定有Cu、Ag;滤渣与稀盐酸反应的化学方程式为Fe+2HCl═FeCl2+H2↑;由于稀硝酸具有强氧化性,所以滤液中的溶质是Fe(NO3)2.
故答案为:(1)Cu
(2)与水和氧气接触;3CO+Fe2O3
| ||
(3)Fe、Cu、Ag;Fe+2HCl═FeCl2+H2↑;Fe(NO3)2
点评:本题考查物质的鉴别与推断.用观察法鉴别:Ag、Cu、Fe和Al四种金属中Cu是黑色金属,不是银白色的.

练习册系列答案
相关题目