题目内容
(2013?市中区三模)科学家伽利略说:“一切推理都必须从观察与实验中得来”,以下是老师提供的一些实验装置,请根据要求回答下列问题:

(1)用大理石和稀盐酸反应(稀盐酸挥发出的HCl气体可用饱和NaHCO3溶液吸收)制取并收集干燥纯净的二氧化碳气体.
①关闭 A装置中的止水夹后,从长颈漏斗向锥形瓶中注入一定量的水,静止后如图所示,则A装置是否漏气?
②实验室制取二氧化碳的化学方程式是
③所选仪器的连接顺序
(2)某同学欲用含有二氧化碳和水蒸气杂质的 CO测定一种铁的氧化物(FexOy)的组成,称量该铁的氧化物的质量为 23.2g.设计实验方案:气体流向是从左向右,选择的仪器按 B→C→F→D 顺序连接,然后进行实验(假设有关反应均反应完全…).
①装置B的作用是
②F装置中的FexOy全部被还原后,称量剩余固体的质量为16.8g,该铁的氧化物的化学式为
③用上述方法测量时,如果没有B装置,测定结果中铁元素与氧元素的质量比值会
④该套装置中有一个明显的不足之处,应在装置D后放置燃着的酒精灯处理尾气,这样做的目的是

(1)用大理石和稀盐酸反应(稀盐酸挥发出的HCl气体可用饱和NaHCO3溶液吸收)制取并收集干燥纯净的二氧化碳气体.
①关闭 A装置中的止水夹后,从长颈漏斗向锥形瓶中注入一定量的水,静止后如图所示,则A装置是否漏气?
不漏气
不漏气
(填“漏气”、“不漏气”或“无法确定”之一).②实验室制取二氧化碳的化学方程式是
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
.③所选仪器的连接顺序
A→E→C
A→E→C
→气体收集装置(填写仪器序号字母).(2)某同学欲用含有二氧化碳和水蒸气杂质的 CO测定一种铁的氧化物(FexOy)的组成,称量该铁的氧化物的质量为 23.2g.设计实验方案:气体流向是从左向右,选择的仪器按 B→C→F→D 顺序连接,然后进行实验(假设有关反应均反应完全…).
①装置B的作用是
除去二氧化碳
除去二氧化碳
.②F装置中的FexOy全部被还原后,称量剩余固体的质量为16.8g,该铁的氧化物的化学式为
Fe3O4
Fe3O4
.③用上述方法测量时,如果没有B装置,测定结果中铁元素与氧元素的质量比值会
基本不变
基本不变
(填“偏大”“偏小”“基本不变”之一).④该套装置中有一个明显的不足之处,应在装置D后放置燃着的酒精灯处理尾气,这样做的目的是
防止一氧化碳污染空气
防止一氧化碳污染空气
.分析:(1)①从图中可以看出在密闭的容器中,可以根据压强来判断分析,液面没有下降;
②根据实验室制取CO2气体的药品时大理石和稀盐酸反应产生氯化钙、水和二氧化碳,写出反应的方程式;
③根据二氧化碳的性质可以知道干燥可以用浓硫酸,而吸收氯化氢气体可以用饱和的碳酸钠溶液,可以据此来解答该题;
(2)①根据题意和装置进行分析,各装置设计的目的进行解答;
②根据对所测装置质量的分析(C装置减少的质量就是氧化物中氧元素的质量),计算铁的氧化物中所含铁元素与氧元素的质量,根据铁的氧化物中铁元素和氧元素的质量比求出氧化物的化学式;
③分析为测定铁的氧化物的组成各装置的作用,对各装置进行评价,并判断对测定结果所产生的影响;
④因为CO具有毒性,所以在实验中要将尾气CO进行无害化处理.
②根据实验室制取CO2气体的药品时大理石和稀盐酸反应产生氯化钙、水和二氧化碳,写出反应的方程式;
③根据二氧化碳的性质可以知道干燥可以用浓硫酸,而吸收氯化氢气体可以用饱和的碳酸钠溶液,可以据此来解答该题;
(2)①根据题意和装置进行分析,各装置设计的目的进行解答;
②根据对所测装置质量的分析(C装置减少的质量就是氧化物中氧元素的质量),计算铁的氧化物中所含铁元素与氧元素的质量,根据铁的氧化物中铁元素和氧元素的质量比求出氧化物的化学式;
③分析为测定铁的氧化物的组成各装置的作用,对各装置进行评价,并判断对测定结果所产生的影响;
④因为CO具有毒性,所以在实验中要将尾气CO进行无害化处理.
解答:解:(1)①若装置漏气,装置内的气体向外逸出,装置内的气体压强减小,在外界大气压的作用下长颈漏斗内的液面将会下降,而现在装置内的液面没有下降,说明装置不漏气;
②实验室制取CO2气体的药品时大理石和稀盐酸,反应产生氯化钙、水和二氧化碳,该反应化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑;
③发生装置是固液反应的A装置,除水用浓硫酸,除去氯化氢用饱和碳酸氢钠溶液,如果先除掉水后,再通过碳酸氢钠溶液时会又带上水,前面的水就白除了,所以把除水放在最后除,要先通过饱和碳酸氢钠溶液除去氯化氢,再通过浓硫酸除水,最后收集,故连接顺序为:A→E→C;
(2)①其中B装置装NaOH目的是将一氧化碳(含少量二氧化碳)中的二氧化碳除去,以免影响实验结果;
②完全反应后,装置C中剩余固体质量16.8g,即铁的氧化物中铁的质量;而装置C减少的质量为氧化物中氧元素的质量,23.2g-16.8g=6.4g;
设则该铁的氧化物化学式为FexOy,氧化物中铁元素和氧元素的质量比为:
=
,整理得
=
,所以该铁的氧化物的化学式是Fe3O4;
③装置B是除去混合气体中的二氧化碳,对C装置的质量变化并无影响,所以对测定铁的氧化物的化学式结果无影响;
④因为一氧化碳有毒,会污染空气,因此装置D后放置燃着的酒精灯处理尾气的目的是:防止一氧化碳污染空气;
故答案为:(1)不漏气;CaCO3+2HCl=CaCl2+H2O+CO2↑;A→E→C;
(2)除去二氧化碳;Fe3O4;基本不变;防止一氧化碳污染空气.
②实验室制取CO2气体的药品时大理石和稀盐酸,反应产生氯化钙、水和二氧化碳,该反应化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑;
③发生装置是固液反应的A装置,除水用浓硫酸,除去氯化氢用饱和碳酸氢钠溶液,如果先除掉水后,再通过碳酸氢钠溶液时会又带上水,前面的水就白除了,所以把除水放在最后除,要先通过饱和碳酸氢钠溶液除去氯化氢,再通过浓硫酸除水,最后收集,故连接顺序为:A→E→C;
(2)①其中B装置装NaOH目的是将一氧化碳(含少量二氧化碳)中的二氧化碳除去,以免影响实验结果;
②完全反应后,装置C中剩余固体质量16.8g,即铁的氧化物中铁的质量;而装置C减少的质量为氧化物中氧元素的质量,23.2g-16.8g=6.4g;
设则该铁的氧化物化学式为FexOy,氧化物中铁元素和氧元素的质量比为:
| 56x |
| 16y |
| 16.8g |
| 6.4g |
| x |
| y |
| 3 |
| 4 |
③装置B是除去混合气体中的二氧化碳,对C装置的质量变化并无影响,所以对测定铁的氧化物的化学式结果无影响;
④因为一氧化碳有毒,会污染空气,因此装置D后放置燃着的酒精灯处理尾气的目的是:防止一氧化碳污染空气;
故答案为:(1)不漏气;CaCO3+2HCl=CaCl2+H2O+CO2↑;A→E→C;
(2)除去二氧化碳;Fe3O4;基本不变;防止一氧化碳污染空气.
点评:(1)熟记实验室制取二氧化碳的反应原理、实验步骤、装置示意图、注意事项以及物质的检验和除杂的知识,本题容易出错的地方是连接顺序,要熟记除杂质时导管要遵循“长进短出”的原则,在除水时要放到最后除,否则再通过其他试液时又会带上水;
(2)本题是一道探究性实验题,它以课本的一氧化碳还原氧化铁为依据,尝试了知识的变化角度和迁移能力的考查,CO的还原性可以将铁的氧化物中的铁还原出来,根据实验目明确所设计的实验装置的作用,同时注意一氧化碳的毒性,要进行无害处理,避免环境污染.
(2)本题是一道探究性实验题,它以课本的一氧化碳还原氧化铁为依据,尝试了知识的变化角度和迁移能力的考查,CO的还原性可以将铁的氧化物中的铁还原出来,根据实验目明确所设计的实验装置的作用,同时注意一氧化碳的毒性,要进行无害处理,避免环境污染.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
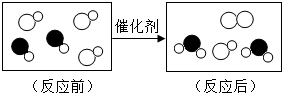 (2013?市中区三模)“尾气催化转化器”可以将汽车尾气中有毒气体转变为无毒气体,如图所示是其中一个化学 反应的微观示意图,其中不同的圆球代表不同的原子.从图中获得信息不正确的是( )
(2013?市中区三模)“尾气催化转化器”可以将汽车尾气中有毒气体转变为无毒气体,如图所示是其中一个化学 反应的微观示意图,其中不同的圆球代表不同的原子.从图中获得信息不正确的是( )