题目内容
【题目】某学习小组对人体吸入的空气与呼出的气体,进行了如下探究
【提出问题】 人体吸入的空气与呼出的气体组成有什么不同?
【查阅资料】
通常条件下,白磷与氢氧化钠溶液不反应.
【实验操作、记录、分析】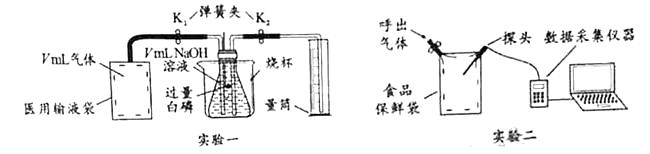
实验一:
(1)先检查装置的 , 装入试剂,在医用输液袋中装入Vml 气体,连接 装置.
(2)打开弹簧夹 , 缓慢将袋中的气体全部排除.读出量筒中液体体积为V1mL。氢氧化钠发生反应的化学方程式是.
(3)关闭弹簧夹 K1、K2 , 再(填操作方法),以促使白磷迅速燃烧。 待瓶中气体冷却至室温,打开 K2.读出量筒中液体体积为 V2ml,其数值等于已反应的之外的气体总体积.
实验二:
(4)把氧气、二氧化碳、水蒸气(测湿度)探头放入袋中,开始采集数据,然后向袋内呼出气体。采集的数据经处理如图,表示二氧化碳体积分数变化的是(填“X”、“Y”、“Z”)。Y 的体积分数在 60s 之后逐渐减小的原因是.
(5)实验一中,二氧化碳的体积分数是 , 氧气的体积分数是.
(6)实验二中,200s 时没有采集数据的所有气体的总体积分数为.
(7)【评价与反思】
有人认为教材中空气成分的“其它气体和杂质”主要是指水蒸气,由实验二判断此说法是 , (填“正确”或“错误”)的,理由是.
【答案】
(1)气密性
(2)K1、K2,2NaOH+CO2=Na2CO3+H2O
(3)向烧杯中加入热水,O2、CO2
(4)Z,水蒸气冷凝【数据处理】
(5)(V-V1)/V×100%,(V1- V2)/V×100%
(6)76.66%
(7)错误,由实验 2 可知,空气中水的体积分数为 1.98%,而空气成分的气体杂质体积分数为 0.03%
【解析】(1)先检查装置的气密性;(2)打开弹簧夹K1、K2,缓慢将袋中的气体全部排除。读出量筒中液体体积为V1ml。氢氧化钠与二氧化碳反应生成碳酸钠和水,化学方程式是2NaOH+CO2=Na2CO3+H2O;(3)燃烧需要满足的条件是可燃物,氧气,温度达到可燃物的着火点。白磷是可燃物,空气中有氧气,还需要的条件是温度达到可燃物的着火点。故进行的操作是向烧杯中加入热水;燃烧需要消耗氧气,与氢氧化钠反应需要消耗二氧化碳。故读出量筒中液体体积为 V2ml,其数值等于已反应的O2、CO2 之外的气体总体积;(4)人体呼出气体的主要成分是氧气、二氧化碳、水蒸气,且氧气含量减少,二氧化碳与水蒸气含量增大,二氧化碳的含量大于水蒸气的含量,故Z表示二氧化碳体积分数变化;Y 的体积分数在 60s 之后逐渐减小的原因是水蒸气冷凝;(5)二氧化碳的体积为(V-V1) ml,其体积分数为 ![]() ;氧气的体积是(V1- V2),其体积分数为
;氧气的体积是(V1- V2),其体积分数为 ![]() ;(6)气体的总质量分数为100%,其中x占17.17%,y占2.50%,z占3.67%,故实验二中,200s 时没有采集数据的所有气体的总体积分数为100%-17.17%-2.50%-3.67%=76.66%;(7)有人认为教材中空气成分的“其它气体和杂质”主要是指水蒸气,由实验二判断此说法是错误的;理由是由实验 2 可知,空气中水的体积分数为 1.98%,而空气成分的气体杂质体积分数为 0.03%.
;(6)气体的总质量分数为100%,其中x占17.17%,y占2.50%,z占3.67%,故实验二中,200s 时没有采集数据的所有气体的总体积分数为100%-17.17%-2.50%-3.67%=76.66%;(7)有人认为教材中空气成分的“其它气体和杂质”主要是指水蒸气,由实验二判断此说法是错误的;理由是由实验 2 可知,空气中水的体积分数为 1.98%,而空气成分的气体杂质体积分数为 0.03%.
所以答案是:(1)气密性;(2)K1、K2;2NaOH+CO2=Na2CO3+H2O;(3)向烧杯中加入热水;O2、CO2;(4)Z;水蒸气冷凝;(5)(V-V1)/V×100%;(V1- V2)/V×100%;(6)76.66%;(7)错误;由实验 2 可知,空气中水的体积分数为 1.98%,而空气成分的气体杂质体积分数为 0.03%.

