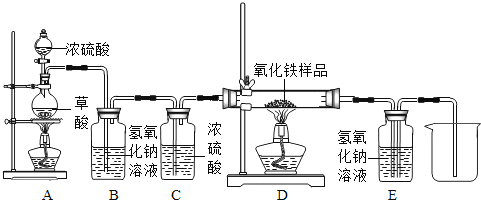
��Ŀ����
����Ŀ����ʵ����ϣ�ͬѧ����п��ϡ���ᷴӦ��ȡ������С��ȡ��Ӧ�����Һ164.7g������̼������Һ���Ⱥ�������Ͱ�ɫ�������ɣ�����̼������Һ�����ɳ����������������ϵ��ͼ��
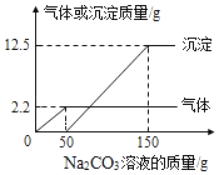
��1������̼������Һ�����ɵ�������_____��
��2��̼������Һ��̼���Ƶ���������Ϊ_____������������ȷ��0.1%����ͬ��
��3��������150g̼������Һʱ��������Һ�����ʵ���������Ϊ����_____������3��д��������̣�
���𰸡�CO2�� 10.6% 7.1%��
��������
��1�������ķ�Ӧ�У�Na2CO3+H2SO4��Na2SO4+H2O+CO2����Na2CO3+ZnSO4��ZnCO3��+Na2SO4�������ɵ������Ƕ�����̼���ʴ�Ϊ��CO2��
�����ᷴӦ����̼���Ƶ�����Ϊx�����������Ƶ�����Ϊy������п��Ӧ����̼���Ƶ�����Ϊm�����������Ƶ�����Ϊn��
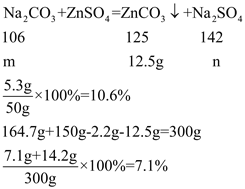
���x��5.3g��y��7.1g��
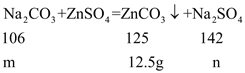
��![]() �����m��10.6g��n��14.2g��
�����m��10.6g��n��14.2g��
��2��̼������Һ��̼���Ƶ���������Ϊ��![]()
��̼������Һ��̼���Ƶ���������Ϊ10.6%��
��3����Ӧ����Һ��������![]() �������Ƶ�����������
�������Ƶ�����������![]()
��������Һ�������Ƶ���������Ϊ7.1%��

 �����Ļ���������人������ϵ�д�
�����Ļ���������人������ϵ�д� ���������ּ���ÿһ��ȫ�º�����ҵ��ϵ�д�
���������ּ���ÿһ��ȫ�º�����ҵ��ϵ�д�����Ŀ��ij��ѧ��ȤС��Ϊ��̽���¶ȶ�H2O2�ֽⷴӦ���ʵ�Ӱ�죬������ͼ��ʾʵ��װ�ã�����������ʵ�飬����ʵ��IJ�����������ʾ��
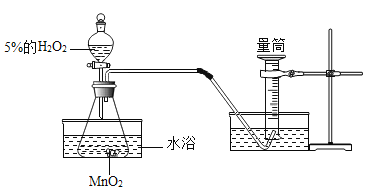
ʵ��1 | ʵ��2 | |
MnO2������/�� | 0.5 | 0.5 |
5%��H2O2���/���� | 40 | ���� |
ˮԡ�¶�/�� | 20 | 80 |
��ܰ��ʾ����ʵ���е���ˮԡ����ָͨ��ˮ���е���ˮ���������ݵ���Ҫ���ȵ���ƿ��ﵽ���ȵ�Ŀ�ġ�
��1����ʵ�����ռ�����ķ�����_____��
��2��ʵ��2����������������ӦΪ_____��
��3��ʵ���������Ҫ��MnO2�ӻ�����з���������ɲ�ȡ���²�����_____��ϴ�ӡ����
��4��������ʵ���У���ͨ��_____���Ƚ�H2O2�ֽⷴӦ���ʵĴ�С��
��5�������йظ�ʵ���˵������ȷ����_____��������ţ�
A �����Ӷ�������ᵼ�²�õ��������ƫ��
B ��ƿ��ԭ�еĿ���������Ͳ�ᵼ�²�õ��������ƫ��
C ʵ�������������������Ҿ��Ȳ���ʱ���ܽ������쵽��Ͳ�ڽ����ռ�����ⶨ���
D ʵ��2�������¶Ƚϸ�ʹ�����������ͣ��ᵼ�²�õķֽ����ʱ�ʵ�ʿ�
����Ŀ������������ѧϰ��ѧ���õķ�����
��1����ѧʵ�鰴���о����ݿɷ�Ϊ����ѧ����������ʵ�顢���ʵ����ʵ�ʵ�顢��ʾ��ѧ���������ԭ�������ɣ���ʵ��ȡ��ݴ�Ӧ������ʵ���е�B��_____���������Ϊһ�࣬������_____��
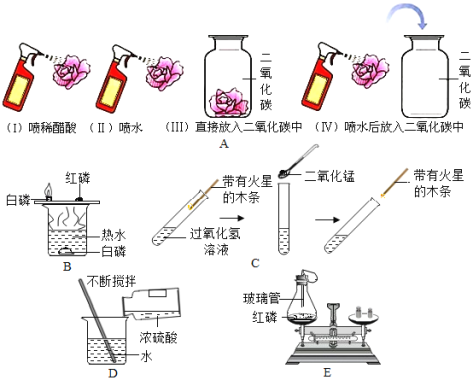
��2��ͨ���۲�����е���Ϣ������Ԫ�صĻ��ϼ���ԭ�ӵ������������Ĺ�ϵ�����ܷ����й�Ԫ�ػ��ϼ۵Ĺ�����_____��Ӧ�ô˹��������Ʋ����Ԫ�ص��������_____����������Ԫ����+5�ۣ�������Ļ�ѧʽΪ_____��
Ԫ������ | ��������ϼ� | ������ϼ� |
�� | +6 | ��2 |
�� | +7 | ��1 |