题目内容
(2010?杨浦区一模)过氧化氢溶液常用于实验室制取氧气.可供选择的仪器或装置如下图所示.
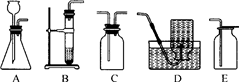
(1)要收集干燥的氧气,整套装置的连接顺序为(由气体发生装置开始)
(2)加入药品通常采用“把过氧化氢溶液缓缓加入盛有少量MnO2的反应容器中”,优点是
(3)MnO2可以连续反应使用,理由是
(4)根据化学方程式计算获得的氧气理论值总是比实际实验操作收集到气体的数值大(若装置不漏气且实验操作正确),原因是
(5)生产火箭燃料的工业废水中含有少量偏二甲肼X,可用双氧水处理排污,反应的化学方程式为X+8H2O2→2CO2↑+N2↑+12H2O,则X的化学式为

(1)要收集干燥的氧气,整套装置的连接顺序为(由气体发生装置开始)
ACE
ACE
(选填字母A~E);(2)加入药品通常采用“把过氧化氢溶液缓缓加入盛有少量MnO2的反应容器中”,优点是
氧气能够均匀连续的放出
氧气能够均匀连续的放出
;(3)MnO2可以连续反应使用,理由是
催化剂的质量和化学性质在反应前后都没有改变
催化剂的质量和化学性质在反应前后都没有改变
;(4)根据化学方程式计算获得的氧气理论值总是比实际实验操作收集到气体的数值大(若装置不漏气且实验操作正确),原因是
当气泡均匀连续的放出时,再收集氧气,氧气跑掉了一部分
当气泡均匀连续的放出时,再收集氧气,氧气跑掉了一部分
.(5)生产火箭燃料的工业废水中含有少量偏二甲肼X,可用双氧水处理排污,反应的化学方程式为X+8H2O2→2CO2↑+N2↑+12H2O,则X的化学式为
C2H8N2
C2H8N2
.分析:本题考查了氧气的实验室制法,制氧气时,可以有两种装置,如果是用高锰酸钾或氯酸钾时,发生装置就需要加热;如果是用过氧化氢溶液和二氧化锰时,发生装置不需要加热.本题是用过氧化氢溶液制氧气,不需要加热,装置B不好控制反应的速度,因此选A,要收集干燥的氧气,用装置C干燥,收集装置只能选用E装置.催化剂的特点是:一变、二不变;根据质量守恒定律,反应前后原子的种类和数目没有变化,可以得出物质的化学式.
解答:解:(1)过氧化氢溶液制氧气,不需要加热,装置B不好控制反应的速度,因此选A,要收集干燥的氧气,用装置C干燥,收集装置只能选用E装置,故答案为:ACE
(2)把过氧化氢溶液缓缓加入盛有少量MnO2的反应容器中,是为了让氧气能够均匀连续的放出,控制反应的速度.故答案为:氧气能够均匀连续的放出
(3)催化剂的质量和化学性质在反应前后都没有改变,因此可以重复使用.故答案为:催化剂的质量和化学性质在反应前后都没有改变
(4)氧气理论值总是比实际实验操作收集到气体的数值大,原因是:当气泡均匀连续的放出时,再收集氧气,氧气跑掉了一部分;还可能溶解在水中少量氧气.故答案为:当气泡均匀连续的放出时,再收集氧气,氧气跑掉了一部分
(5)根据质量守恒定律,反应前后原子的种类和数目没有变化,得出化学式偏二甲肼为:C2H8N2.故答案为:C2H8N2
(2)把过氧化氢溶液缓缓加入盛有少量MnO2的反应容器中,是为了让氧气能够均匀连续的放出,控制反应的速度.故答案为:氧气能够均匀连续的放出
(3)催化剂的质量和化学性质在反应前后都没有改变,因此可以重复使用.故答案为:催化剂的质量和化学性质在反应前后都没有改变
(4)氧气理论值总是比实际实验操作收集到气体的数值大,原因是:当气泡均匀连续的放出时,再收集氧气,氧气跑掉了一部分;还可能溶解在水中少量氧气.故答案为:当气泡均匀连续的放出时,再收集氧气,氧气跑掉了一部分
(5)根据质量守恒定律,反应前后原子的种类和数目没有变化,得出化学式偏二甲肼为:C2H8N2.故答案为:C2H8N2
点评:本考点考查了仪器的名称、气体发生装置的选择,以及干燥的方法、催化剂的特点和质量守恒定律等.实验室三大气体的发生装置和收集装置的选择、验证和验满是中考的重要考点,一定要认真掌握.有关实验评价问题是近几年经常出现的考点之一,要认真分析.本考点的知识点比较多,要加强对比记忆,理解应用,本考点一般出现在实验题中.

练习册系列答案
相关题目