题目内容
2011年3月,日本海啸引发福岛第一核电站的放射性物质外泄,有关131I(碘-131)的相关报道成为热门话题.请回答下列问题:(1)碘元素在体内发挥重要作用,但过量补碘也会引起甲亢等疾病.目前我国各地检测出的131I含量很小,根据京津等地检出的数值,吃上2000kg的菠菜才相当于照一张X光片的辐射量.根据以上资料分析,下列说法正确的是
a.盲目服用碘片等预防辐射对身体可能造成负面作用
b.我们应尽可能主动多摄入含碘食品,多多益善
c.以目前我国检测出的131I含量来看,对身体健康影响很小,不必恐慌
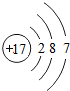
(2)131I原子中含有53个质子,78个中子.
①131I原子的核外电子数为
②自然界中普遍存在另一种稳定的碘原子127I,它和131I同属于碘元素.127I原子的质子数为
(3)专家指出,服用碘片(有效成分为KI)可以治疗131I造成的辐射,但服用碘酒(有效成分为I2)却会引起碘中毒.KI和I2性质的不同的原因是
(4)①食盐中常添加碘酸钾(KIO3)以补充碘元素.已知KIO3中钾元素的化合价为+1,其中碘元素的化合价为
②服用碘片治疗131I辐射的推荐服用剂量是每日摄入KI为130-170mg,假设服用某碘片每日补充166mg KI.已知每千克某品牌碘盐中KIO3的加入量为42.8mg,如果用该食盐替代碘片提供治疗辐射所需的碘元素,则每日需食用该食盐的质量为
分析:(1)利用题中的信息结合所学的化学知识解决.
(2)①根据原子中质子数=核外电子数回答.
②根据元素的种类是由质子数决定的回答.
(3)根据物质的结构决定物质的性质回答.
(4)①利用化合物中元素的化合价代数和等于零解决②根据每日需要补充166mgKI的质量计算所需碘元素的质量,根据碘元素的质量求出碘酸钾的质量,再根据已知每千克某品牌碘盐中KIO3的加入量为42.8mg计算碘盐的质量.
(2)①根据原子中质子数=核外电子数回答.
②根据元素的种类是由质子数决定的回答.
(3)根据物质的结构决定物质的性质回答.
(4)①利用化合物中元素的化合价代数和等于零解决②根据每日需要补充166mgKI的质量计算所需碘元素的质量,根据碘元素的质量求出碘酸钾的质量,再根据已知每千克某品牌碘盐中KIO3的加入量为42.8mg计算碘盐的质量.
解答:解:(1)由题中的信息可以看出,过量服碘有害无益.
(2)①131I原子中含有53个质子,根据原子中质子数=核外电子数,131I原子的核外电子数为53.
②由于元素的种类是由质子数决定的,碘原子127I和131I同属于碘元素,故127I原子的质子数为53.
(3)物质的性质是由物质的结构决定的,KI和I2的性质不同是因构成物质的微粒(分子)不同.
(4)①碘酸钾中碘的化合价可通过钾的化合价是+1氧的化合价是-2,再结合相关的化合物中化合价代数和是零的原则完成,求得碘的化合价是+5;
②KI中碘的质量分数为
×100%=76.5%,每日需要补充166mg KI,则含碘元素的质量为166mg×76.5%=127mg;KIO3中碘的质量分数为
×100%=59.35%,则需碘酸钾
=214mg,已知每千克某品牌碘盐中KIO3的加入量为42.8mg,故每日需食用该食盐的质量为:
=5kg.
故答案为:(1)ac(2)①53;②53;(3)构成物质的微粒(分子)不同(要点是“结构不同”);(4)①+5②5.
(2)①131I原子中含有53个质子,根据原子中质子数=核外电子数,131I原子的核外电子数为53.
②由于元素的种类是由质子数决定的,碘原子127I和131I同属于碘元素,故127I原子的质子数为53.
(3)物质的性质是由物质的结构决定的,KI和I2的性质不同是因构成物质的微粒(分子)不同.
(4)①碘酸钾中碘的化合价可通过钾的化合价是+1氧的化合价是-2,再结合相关的化合物中化合价代数和是零的原则完成,求得碘的化合价是+5;
②KI中碘的质量分数为
| 127 |
| 39+127 |
| 127 |
| 39+127+16×3 |
| 127mg |
| 59.35% |
| 214mg |
| 42.8mg/kg |
故答案为:(1)ac(2)①53;②53;(3)构成物质的微粒(分子)不同(要点是“结构不同”);(4)①+5②5.
点评:本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.学生分析问题的思维跨度较大,强调了学生整合知识的能力,以及对信息的分析、提炼、加工、运用的能力.

练习册系列答案
相关题目
 2011年3月,日本强烈地震后,海啸引发福岛第一核电站的放射性物质外泄,有关131I(碘-131)的相关报道成为热门话题.为避免核辐射,需一次性口服100毫克不具放射性的碘原子(碘-127),使人体甲状腺中碘达到饱和而不再吸收外界的碘,从而起到保护作用.请回答:
2011年3月,日本强烈地震后,海啸引发福岛第一核电站的放射性物质外泄,有关131I(碘-131)的相关报道成为热门话题.为避免核辐射,需一次性口服100毫克不具放射性的碘原子(碘-127),使人体甲状腺中碘达到饱和而不再吸收外界的碘,从而起到保护作用.请回答: