题目内容
三位同学分别设计了由铜制取硫酸铜的如下三种方案.
方案一:铜与浓硫酸直接反应 Cu+2H2SO4(浓)  CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
方案二:Cu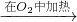 Cu0
Cu0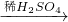 CuSO4
CuSO4
方案三:Cu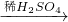 CuSO4
CuSO4
试评价上述三个方案是否合理,不合理的请简要说明理由:
方案一________.
方案二________.
方案三________.
不合理,产生的SO2有毒,污染空气 合理 不合理,铜位于金属活动性顺序表中氢后,与稀硫酸不反应
分析:评价实验方案要从反应的可操作性,生成物的性质,环保节能等方面分析.由于浓硫酸与铜直接反应时会生成有毒的二氧化硫,方案三中因铜的活动性在氢后不会与稀硫酸反应,只有二方案环保并且使用的硫酸量较小,非常合理.
解答:一方案中放出的有毒气体二氧化硫会造成对空气的污染,因此,从保护环境的角度来看,一方案就不够合理;根据生成硫酸铜反应的化学方程式可以看到,生成相同物质的量的硫酸铜,消耗硫酸的物质的量一方案也是二方案有两倍,因此从节约原料的角度来看,一方案也不够合理,三方案该过程无法完成,因为铜的活动性在氢后不会与稀硫酸反应
故答案为:不合理,产生的SO2有毒,污染空气;
合理;
不合理,铜位于金属活动性顺序表中氢后,与稀硫酸不反应
点评:本题既考查了物质的性质、化学方程式的书写,还对反应的化学方程式所反映出的物质的质量关系进行“隐性”考查,是一道综合性较强的方案设计题.
分析:评价实验方案要从反应的可操作性,生成物的性质,环保节能等方面分析.由于浓硫酸与铜直接反应时会生成有毒的二氧化硫,方案三中因铜的活动性在氢后不会与稀硫酸反应,只有二方案环保并且使用的硫酸量较小,非常合理.
解答:一方案中放出的有毒气体二氧化硫会造成对空气的污染,因此,从保护环境的角度来看,一方案就不够合理;根据生成硫酸铜反应的化学方程式可以看到,生成相同物质的量的硫酸铜,消耗硫酸的物质的量一方案也是二方案有两倍,因此从节约原料的角度来看,一方案也不够合理,三方案该过程无法完成,因为铜的活动性在氢后不会与稀硫酸反应
故答案为:不合理,产生的SO2有毒,污染空气;
合理;
不合理,铜位于金属活动性顺序表中氢后,与稀硫酸不反应
点评:本题既考查了物质的性质、化学方程式的书写,还对反应的化学方程式所反映出的物质的质量关系进行“隐性”考查,是一道综合性较强的方案设计题.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
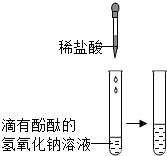
 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O Cu0
Cu0 CuSO4
CuSO4 CuSO4
CuSO4