��Ŀ����
����Ŀ�����껯ѧʵ����������У���һ��Ŀ�Ǽ������ʯ��ˮ������������Һ���������̽���� ��������⡿��μ�����������ɫ��Һ��
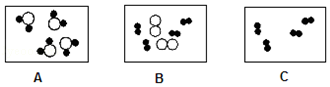
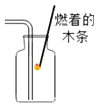
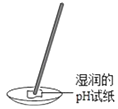
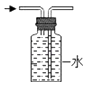
��ʵ�鷽����С���ȼ�λͬѧ��������ͼ��ʾ��ʵ�飮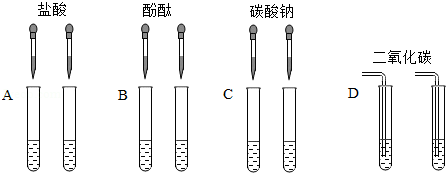
����ش��������⣺
��1��C��ʵ���з�Ӧ�Ļ�ѧ����ʽΪ��
��2�����в��ܴﵽʵ��Ŀ����������ĸ����
��3��D��ʵ���б���ǵ�ԭ��Һ�� ��
��4��������̽����ʵ�������С��ͬѧ��A��B��C��D�����Թ��е�����ȫ������ͬһ���ɾ����ձ��У���ַ�Ӧ�õ���ɫ����������Һ���Ը���Һ�ijɷ��ֽ�����̽���� ��������⡿����Һ�г�ˮ����̪�������Щ���ʣ�
���������ϡ��Ȼ�����Һ�����ԣ�
����������衿
��
��NaCl��CaCl2��HCl
��NaCl��CaCl2��NaOH
����˼����չ�������������������ֻ��һ��������������������ţ��������� ��
�ڸ�����ѧ��ѧ֪ʶ����֤�ձ�����Һ�п����е������Ƿ���ڣ�������Щ���ʵ���ʹ�ò�����ɸ�ʵ��������ĸ��
a��pH��ֽ b����������Һ c����ɫʯ����Һ d��ͭ e����������������Һ��
���𰸡�
��1��Na2CO3+Ca��OH��2�TCaCO3��+2NaOH
��2��A��B
��3������ʯ��ˮ��Ca��OH��2��Һ
��4��NaCl��CaCl2����NaOH��Һ��ʹ��ɫ��̪��Һ��죬���ܵõ���ɫ��Һ�������𰸾��ɣ���b��d
���������⣺��ʵ�鷽������1��̼���ƺ��������Ʒ�Ӧ���ɰ�ɫ��̼��Ƴ������������ƣ���Ӧ�ķ���ʽΪ��Na2CO3+Ca��OH��2�TCaCO3��+2NaOH����2��A��������Ӧ�����������ʲ��ܼ���B��������ɺ�ɫ���ʲ��ܼ��𣻶�C��D���ܳ��ֲ�ͬ��������˲��ܴﵽʵ��Ŀ����A��B����3��������̼���������Ʒ�Ӧ����̼��Ƴ����������������Ʒ�Ӧ������D��ʵ���б���ǵ�ԭ��Һ��ʯ��ˮ������������衿��ǡ����ȫ��Ӧ����ֻ���з�Ӧ�������Ȼ��ƺ��Ȼ��ƣ� ����˼����չ���٢�IJ����к����������ƣ��ܹ�ʹ��̪��Һ��ɺ�ɫ��������õ���ɫ����������Һ����ˢ���������֤�ձ�����Һ�п����е����ʣ�����
a��ͨ��pH��ֽ������֤��Һ�������ԡ����Ի��Ǽ��ԣ��ʿ��ԣ�
b���������ֲ��룬��Ϊ�����������ӣ��μ���������Һ��������������ʲ����ԣ�
c����Ϊ���ֲ�����Һ���ֲ�ͬ�����ʣ���˿���ͨ��ʯ����Һ��֤���ʿ��ԣ�
d��ͭ�����ֲ�������ʶ�����Ӧ���ʲ����ԣ�
e�������͢����μ���������������ɺ�ɫ��˵�����������ᣬ����һ�������ɫ����˵���������ᣬ�ʿ��ԣ�
���b��d�����ԣ�
�ʴ�Ϊ����ʵ�鷽������1����Na2CO3+Ca��OH��2�TCaCO3��+2NaOH����2��A��B����3������ʯ��ˮ��Ca��OH��2��Һ��
����������衿��NaCl��CaCl2��
����˼����չ���٢�NaOH��Һ��ʹ��ɫ��̪��Һ��죬���ܵõ���ɫ��Һ�������𰸾��ɣ�����b��d��
��ʵ�鷽������1�����ݷ�Ӧ��������Լ���Ӧԭ����д����ʽ����2�����ݷ�Ӧ��������м��𣻣�3�����ݶ�����̼���������Ʒ�Ӧ����̼��Ƴ���������
����������衿���ݷ�Ӧ�ij̶ȷ������ʵijɷ֣�
����˼����չ���ٸ�������õ���ɫ����������Һ��������ĺ����ԣ�������֤ʱҪע��ѡ����Լ����ܲ������ţ�Ҫ�������Ե�����