题目内容
(2009?荆门)80g碳酸钠溶液与溶质质量分数为20%的盐酸(密度为1.1g/cm3)恰好完全反应时,整个溶液的质量减少了8.8g.(计算结果保留小数点后一位小数)
(1)反应用去了20%的盐酸多少毫升?
(2)反应后溶液中溶质的质量分数是多少?
(1)反应用去了20%的盐酸多少毫升?
(2)反应后溶液中溶质的质量分数是多少?
分析:(1)根据溶液质量的减少量就是生成二氧化碳的质量,所以生成二氧化碳8.8g,根据二氧化碳的质量算出参加反应的氯化氢的质量,用氯化氢的质量除以20%,算出盐酸溶液质量,再除以盐酸的密度就是用去20%的盐酸的体积;
(2)反应后的溶质是氯化钠,根据二氧化碳的质量算出氯化钠的质量,再计算出反应后总溶液的质量,用氯化钠的质量除以总溶液的质量,即可算出质量分数.
(2)反应后的溶质是氯化钠,根据二氧化碳的质量算出氯化钠的质量,再计算出反应后总溶液的质量,用氯化钠的质量除以总溶液的质量,即可算出质量分数.
解答:解:根据质量守恒定律可知溶液质量的减少量就是生成二氧化碳的质量,所以生成二氧化碳8.8g,设要想生成8.8g二氧化碳,需要参加反应的氯化氢的质量为x,同时生成氯化钠的质量为y:
Na2CO3+2HCl═2NaCl+H2O+CO2↑
73 117 44
x y 8.8g
=
=
x=14.6g,y=23.4g
(1)需要20%的盐酸质量为:
=73g,需要盐酸体积为:
=66.4毫升;
(2)反应后溶质质量为23.4g,反应后溶液质量为:80g+73g-8.8g=144.2g,所以反应后溶液的溶质质量分数为:
×100%=16.2%.
答:(1)反应用去了20%的盐酸66.4毫升;(2)反应后溶液中溶质的质量分数是l6.2%.
Na2CO3+2HCl═2NaCl+H2O+CO2↑
73 117 44
x y 8.8g
| 73 |
| x |
| 117 |
| y |
| 44 |
| 8.8g |
x=14.6g,y=23.4g
(1)需要20%的盐酸质量为:
| 14.6g |
| 20% |
| 73g |
| 1.1g/cm3 |
(2)反应后溶质质量为23.4g,反应后溶液质量为:80g+73g-8.8g=144.2g,所以反应后溶液的溶质质量分数为:
| 23.4g |
| 144.2g |
答:(1)反应用去了20%的盐酸66.4毫升;(2)反应后溶液中溶质的质量分数是l6.2%.
点评:本题容易出错的地方是对反应后溶液质量的计算,有的同学忘记加上盐酸溶液的质量,有的同学忘记减去生成的气体的质量,在进行体积、密度、质量换算时注意单位的统一.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
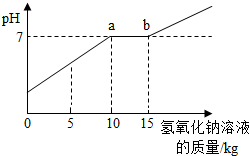 (2009?荆门)通常在实验室做完“氢气的制取”实验后,要将废液倒入废液桶中,这样就可收集一些硫酸和硫酸锌的混合溶液(不考虑其他杂质).为避免污染环境,某校化学兴趣小组的同学做了如下实验:
(2009?荆门)通常在实验室做完“氢气的制取”实验后,要将废液倒入废液桶中,这样就可收集一些硫酸和硫酸锌的混合溶液(不考虑其他杂质).为避免污染环境,某校化学兴趣小组的同学做了如下实验: