题目内容
(2013?黄浦区一模)实验室对氯酸钾和二氧化锰混合制取氧气后的剩余固体进行了如下实验
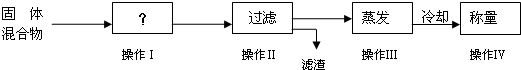
①写出操作Ⅰ的名称
②操作Ⅳ称量所得的固体为1.49g(不计每步操作损耗),请问该实验中氯酸钾和二氧化锰混合加热,产生了多少molO2?(根据化学方程式列式计算)

①写出操作Ⅰ的名称
溶解
溶解
;②操作Ⅳ称量所得的固体为1.49g(不计每步操作损耗),请问该实验中氯酸钾和二氧化锰混合加热,产生了多少molO2?(根据化学方程式列式计算)
分析:要将二氧化锰从混合物中分离出来,首先将固体溶解再进行过滤;根据操作过程可知:操作Ⅳ所得固体为氯化钾,根据氯化钾的质量并结合方程式可减少出生成氧气的物质的量.
解答:解:(1)要将二氧化锰从混合物中分离出来,首先将固体溶解再进行过滤;
故答案为:溶解;
(2)氯化钾的物质的量为:
=0.02mol
设生成O2x mol.
2KClO3
3O2↑+2KCl
3 2
x 0.02mol
=
x=0.03mol
答:生成O20.03mol.
故答案为:溶解;
(2)氯化钾的物质的量为:
| 1.49g |
| 74.5g/mol |
设生成O2x mol.
2KClO3
| ||
| △ |
3 2
x 0.02mol
| 3 |
| x |
| 2 |
| 0.02mol |
x=0.03mol
答:生成O20.03mol.
点评:本题考查了学生获取信息,及利用方程式规范答题的能力,要细心分析,仔细解答.

练习册系列答案
相关题目